67- Ligação Iônica pela Lei de Coulomb
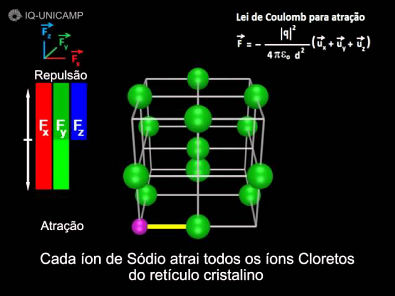

Veja também, Ligação Iônica pela Regra do Octeto de Lewis: http://www.youtube.com/watch?v=0sJl3ijbkSc Para ver a descrição, por favor clique, na aba "Mostrar Mais": A Ligação Iônica, ensinada pela Regra do Octeto de Lewis, apesar de correta, é excessivamente simplicada e isso induz a pensar que: 1- Os íons formam-se a partir de átomos neutros 2- A interação eletrostática ocorre apenas entre dois íons 3- A Ligação Iônica é unidirecional 4- Forma-se uma molécula Poderíamos dizer que o objetivo alcançado, ao ensinar a Ligação Iônica pela Regra do Octeto de Lewis, é mostrar que composto iônicos formam-se porque os íons têm octeto completo. Uma forma ampliada de ensinar a Ligação Iônica, usando a Lei de Coulomb, mostra que: 1- É irrelevante saber como os íons são formados 2- Os íons estão organizados tridimensionalmente num retículo cristalino 3- Cada íon interage eletrostáticamente com todos os outros íons do retículo cristalino 4- A força eletrostática resultante sobre cada íon é calculada pela Lei de Coulomb 5- O retículo cristalino é coeso porque a força eletrostática resultante, calculada para cada íon, mostra que este é atraido pelos demais íons
Compartilhar