Química Orgânica e Analítica
Sobre o indicador fluoresceína mostrados em suas diversas formas iônicas em equilíbrio químico na Figura a seguir, assinale a alternativa que contém assertiva correta sobre as suas propriedades e uso como indicador de precipitação.

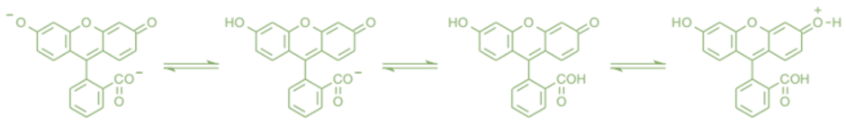
Fonte: Elaborada pela autora (2020).
Os derivados de flouresceína que tem um valor medido de pH e pka de aproximadamente 8 e 6.9, respectivamente, são considerados indicadores do tipo ácido. Esse indicador apresenta a sua ionização com quantidade de sua forma concentração aniônica que é responsável pela solubilidade em água e coloração tão reduzida que torna a análise por titulometria inviável por não apresentar mudança no ponto final visível o suficiente para a que a medida volumétrica possa ser realizada.
A fluoresceína e muitos de seus derivados exibem múltiplos equilíbrios iônicos dependentes do pH.
Os grupos funcionais fenol e ácido carboxílico da fluoresceína são quase totalmente ionizados em soluções aquosas acima de pH 9. Acidificação do ânion de fluoresceína primeiro protona o fenol (pKa ~ 6,4) para produzir o monoânion, então o ácido carboxílico (pKa <5) para produzir a espécie neutra de fluoresceína. A acidificação adicional gera um cátion (pKa ~ 2,1).
Somente os mono-ânion e di-ânion de fluoresceina são fluorescente.
Escolha uma opção:
Apenas II, III e IV são verdadeiras.
Todas são falsas.
Apenas I e II são verdadeiras.
Apenas I, II e III são verdadeiras.
Todas são verdadeiras.
💡 1 Resposta
Elediana Santos
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas dessa disciplina
Conteúdos escolhidos para você
 3 pág.
3 pág. 68 pág.
68 pág.





Compartilhar