o ion iodeto reage com ion hipoclorito da seguinte forma ocl+I-----OI +CL ESCREVE LEI DA VELOCIDADE PARA ESSA REAÇAO
💡 2 Respostas
RD Resoluções
Temos os dados:

Verificando o que ocorre com a velocidade da reação quando é dobrada a quantidade de OCl na reação, é possível perceber que a velocidade da reação aumenta proporcionalmente e com a mesma proporção. Isso mostra que a reação é de ordem 1 em relação a OCl
Logo temos:
\(\[\begin{align} & v=k.{{(OC{{l}^{-}})}^{l}}.{{({{I}^{-}})}^{l}} \\ & v=k.(OC{{l}^{-}}).({{I}^{-}}) \\ \end{align}\] \)
Portanto:
A lei da velocidade é dada por:
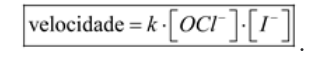
Luísa Souza
Reação de primeira ordem em relação aos dois reagentes, e de segunda ordem global.
CLAUDIONICE GONÇALVES DE SENA
V=K[OCI-][I-]
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 4 pág.
4 pág. 1 pág.
1 pág.




Compartilhar