Que é um orbital hibrido? Por que é necessário utilizer orbitais híbridos para justificar a estrutura do metano?
💡 2 Respostas
Pedro Souza
Orbital hibrido ou hibridização é o processo de formação de orbitais eletrônicos hibridos, os subníveis mais atômicos(s e p) de alguns átomos se misturam formando hibridos; sp, sp², sp³, como no caso do metano.
Especialistas PD
Hibridização ou Hibridação de orbitais é uma interpenetração (mistura) que dá origem a novos orbitais, (de maneira favorável à formação de uma geometria adequada para a ligação) em igual número, denominados orbitais híbridos. A hibridização é determinada pelo arranjo.
Para começar a entender o conceito de hibridização, vamos ver o caso do carbono. Sabe-se que a única forma do carbono efetuar suas 4 ligações é por meio de seus elétrons (desemparelhados) em seus orbitais atômicos. Isso pode ser observado abaixo, com a distribuição eletrônica do carbono e sua distribuição nos orbitais:
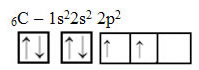
É possível perceber que no orbital 2p, existem somente 2 elétrons desemparelhados (sozinhos) e um orbital totalmente vazio. Dessa forma, o carbono só poderia se ligar duas vezes. Mas não é isso que acontece. A explicação para sua tetravalência se dá pelo fato de o átomo de carbono ter, antes da reação, um dos elétrons 2s promovido ao subnível 2p.
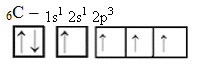
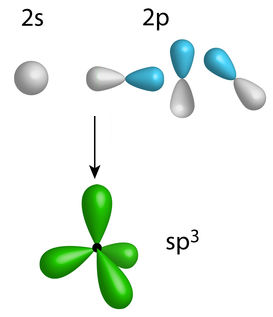
Agora temos 4 elétrons desemparelhados nos orbitais do carbono e esperando novos elétrons para efetuar as ligações. Em seguida, os três orbitais do subnível p unem-se ao orbital do subnível s, resultando então em novos quatro orbitais, que são denominados orbitais híbridos sp3, assim justificando a estrutura do metano.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Bom dia! Por que é necessário utilizar os orbitais híbridos para justificar a estrutura do metano, CH4?
Quimica Organica I Pratica Lab e Ens Quimica
•UFMA
Na Trave!
Materiais relacionados
 16 pág.
16 pág.






Compartilhar