quimica
Compare os elementos Na, Mg, O e P. a) Qual tem maior raio atômico? Justifique sua resposta. b) Qual tem a maior afinidade eletrônica? Justifique sua resposta. c) Coloque os elementos na ordem crescente de energia de ionização. Justifique sua resposta
💡 1 Resposta
Especialistas PD
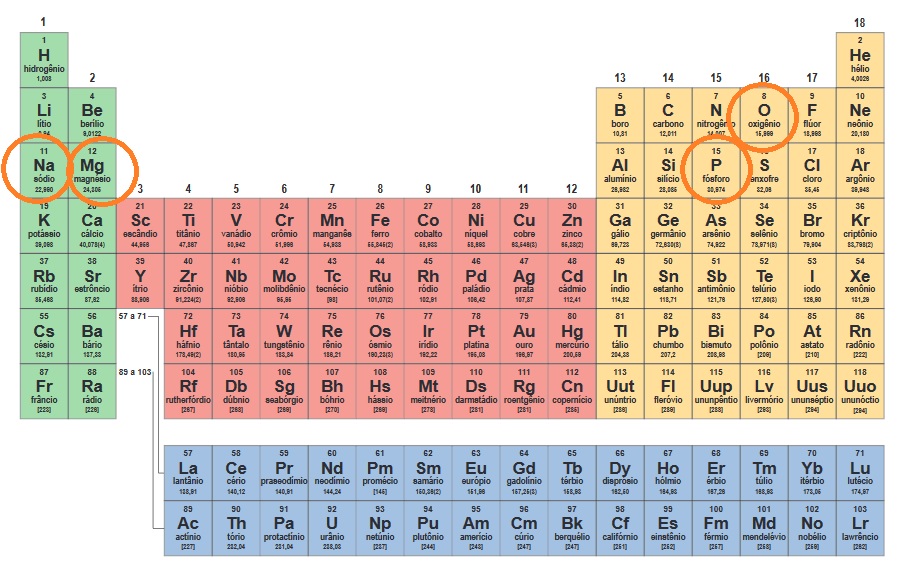
O maior raio atômico é do sódio, pois possui 3 camadas eletrônicas (3º período da tabela periódica) e o menor número atômico. Pois em um mesmo período, quanto maior o número atômico, maior a carga nuclear e maior a atração do núcleo pelos elétrons, assim diminuindo o raio.
A maior afinidade eletrônica é do oxigênio. Afinidade Eletrônica é a energia que um átomo, em estado fundamental, no estado gasoso, libera ao "ganhar" um elétron. Quanto menor o raio, maior é a afinidade eletrônica. O oxigênio, com 2 camadas (2º período da tabela periódica) é o que possui menor raio.
Energia de Ionização é a energia essencial para remover um elétron de um átomo na fase gasosa. Então quanto menor o raio, mais atraído estará o elétron pelo núcleo, então maior será a energia para removê-lo. E energia de ionização é o inverso do raio! Ordem crescente de energia de ionização: Na < Mg < P < O
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
escreva uma tabela descrevendo as propriedades das particulas subatomicas
Química
•ESAMC DE UBERLÂNDIA
maycon garcia




Compartilhar