O que é energia de ativação?
Respostas
Larissa Silva
há 6 anos
Energia de ativação é a energia mínima para que uma reação química possa ocorrer, ou seja, é um dos fatores determinantes para a ocorrência de uma reação, juntamente com o contato e a colisão favorável entre as moléculas dos reagentes.


Crie sua conta grátis para liberar essa resposta. 🤩
Já tem uma conta?
Ao continuar, você aceita os Termos de Uso e Política de Privacidade
Andre Smaira
há 6 anos
---
De maneira básica, a energia de ativação é um tipo de energia necessário para fazer acontecer uma reação química.
Para realizar o cálculo da energia de ativação, é necessário subtrair a entalpia do complexo ativado da entalpia dos reagentes presentes na reação. Então, temos que: \({E_{at}} = {H_{complxAt}} - {H_{reag}}\).
Esta energia de ativação é analisada através de gráficos.
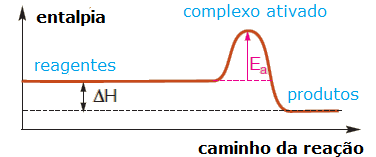
Exemplo de gráfico de energia de ativação
Esta energia de ativação pode ser alterada através de catalisadores, que são ferramentas que diminuem está energia para fazer com que a reação aconteça.
---
Portanto, a energia de ativação é, basicamente, uma energia que é requerida para fazer com que uma reação química ocorra.
Ainda com dúvidas?
Essa pergunta também está no material:
Mais perguntas desse material


