Qual e uma diferença entre cis e trans?
💡 6 Respostas
Monique Silveira
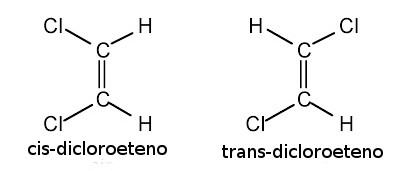
A diferença é que nos isômeros cis, os ligantes estão sempre do mesmo lado do plano, já os isômeros trans estão em lados opostos, por exemplo como na imagem a seguir:
Andre Smaira
Um isômero trans possui moléculas com dois átomos iguais, mas no lado oposto da ligação dupla. O ponto de ebulição é comparativamente baixo para o isômero trans, pois não há forças de atração fortes.
Geralmente, o isomerismo cis e trans pode ser encontrado em compostos orgânicos e inorgânicos, alcanos e alcenos. O isômero cis é um isômero em que dois dos mesmos átomos estão do mesmo lado da ligação dupla em uma molécula.
Um isômero trans consiste em molécula com dois átomos iguais, mas aqui os átomos estão no lado oposto da ligação dupla. Os isômeros trans e cis têm a mesma fórmula molecular e peso molecular, mas diferem em alguns aspectos.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 5 pág.
5 pág.



Compartilhar