(UERJ 2016) Em um experimento, a energia elétrica gerada por uma pilha de Daniell
foi utilizada para a eletrólise de 500 mL de uma solução aquosa de AgNO\(_3\), na concentração de 0,01 mol.L\(^{-1}\).
Observe o esquema:
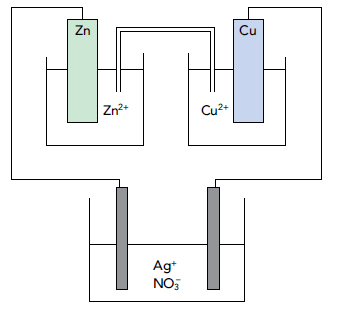
A pilha empregou eletrodos de zinco e de cobre, cujas semirreações de redução são:
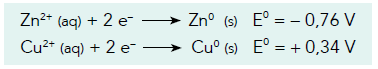
A eletrólise empregou eletrodos inertes e houve deposição de todos os íons prata contidos na solução de AgNO\(_3\).
Calcule a diferença de potencial da pilha, em volts, e a massa, em gramas, do anodo consumido na deposição.
💡 3 Respostas
Estudante PD
Cálculo do potencial da pilha:
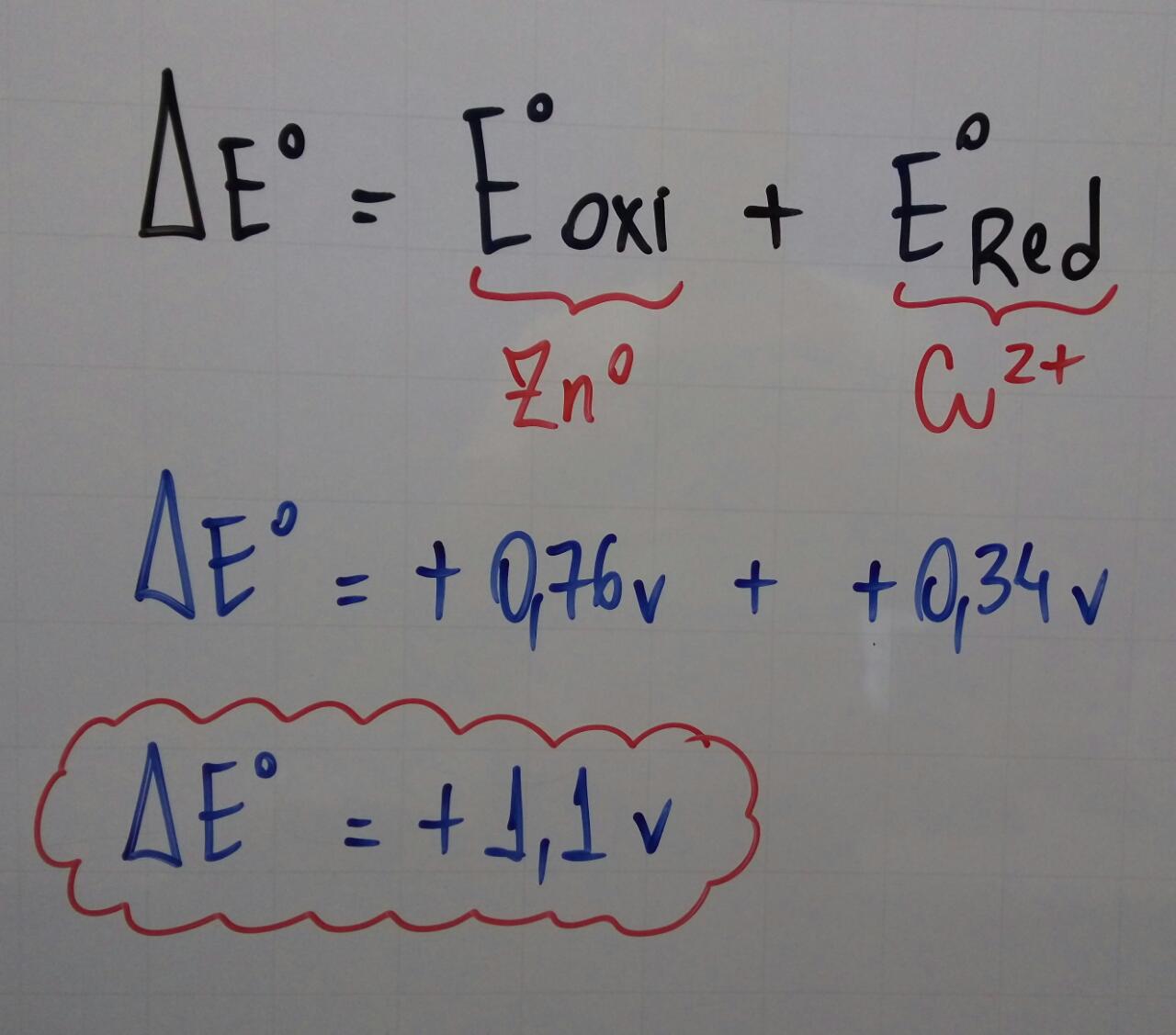
Cálculo da massa de zinco consumida:
1) Cálculo do número de mols de Ag+ (em 500 mL) que reduz:
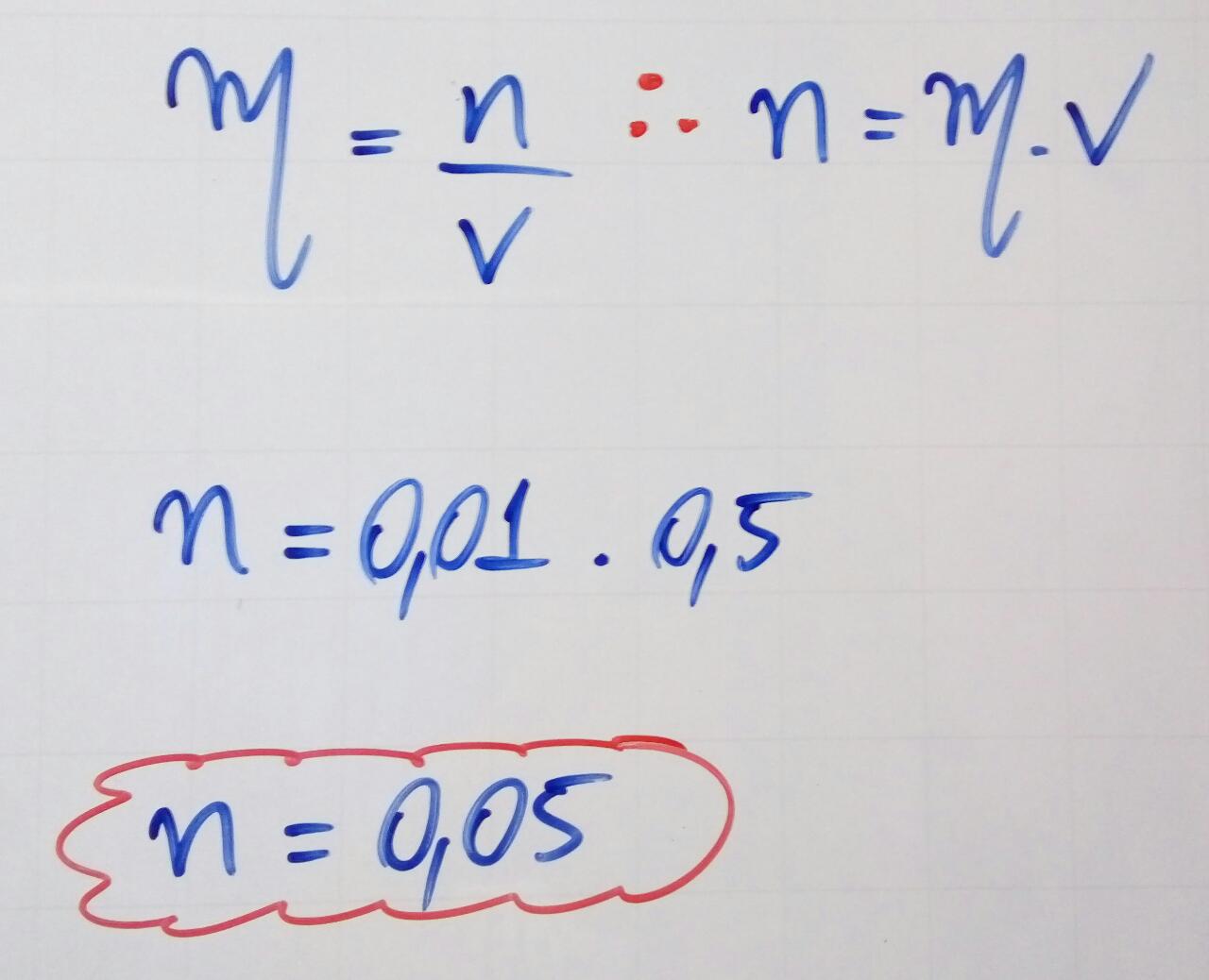
2) Relação molar de reação entre Zn e Ag+:
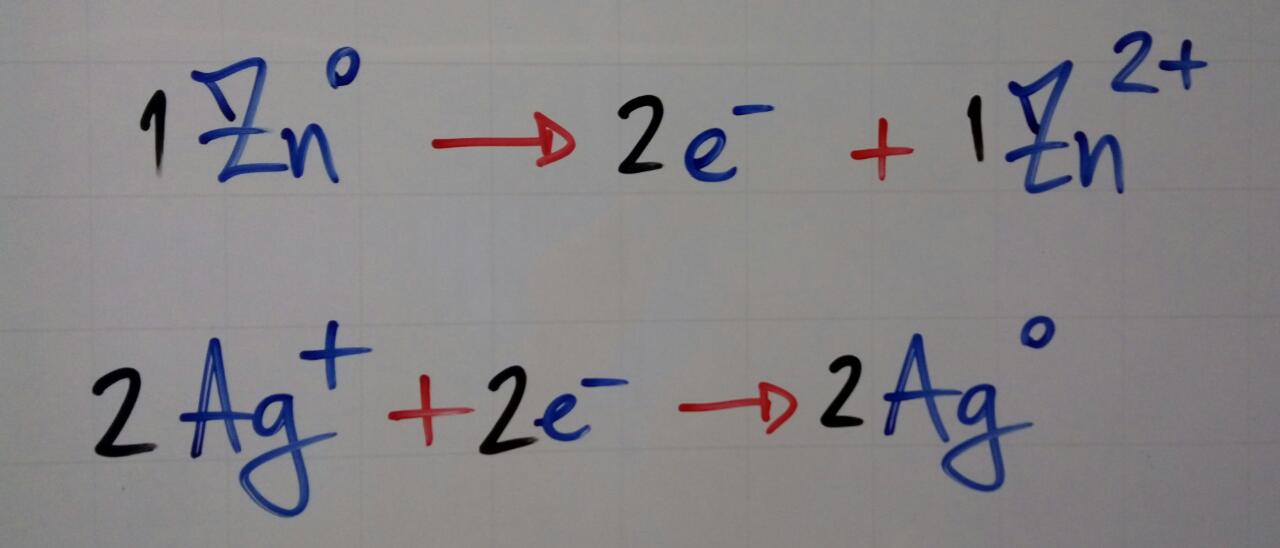
3) Cálculo da massa de Zn através da proporção e de sua massa molar:
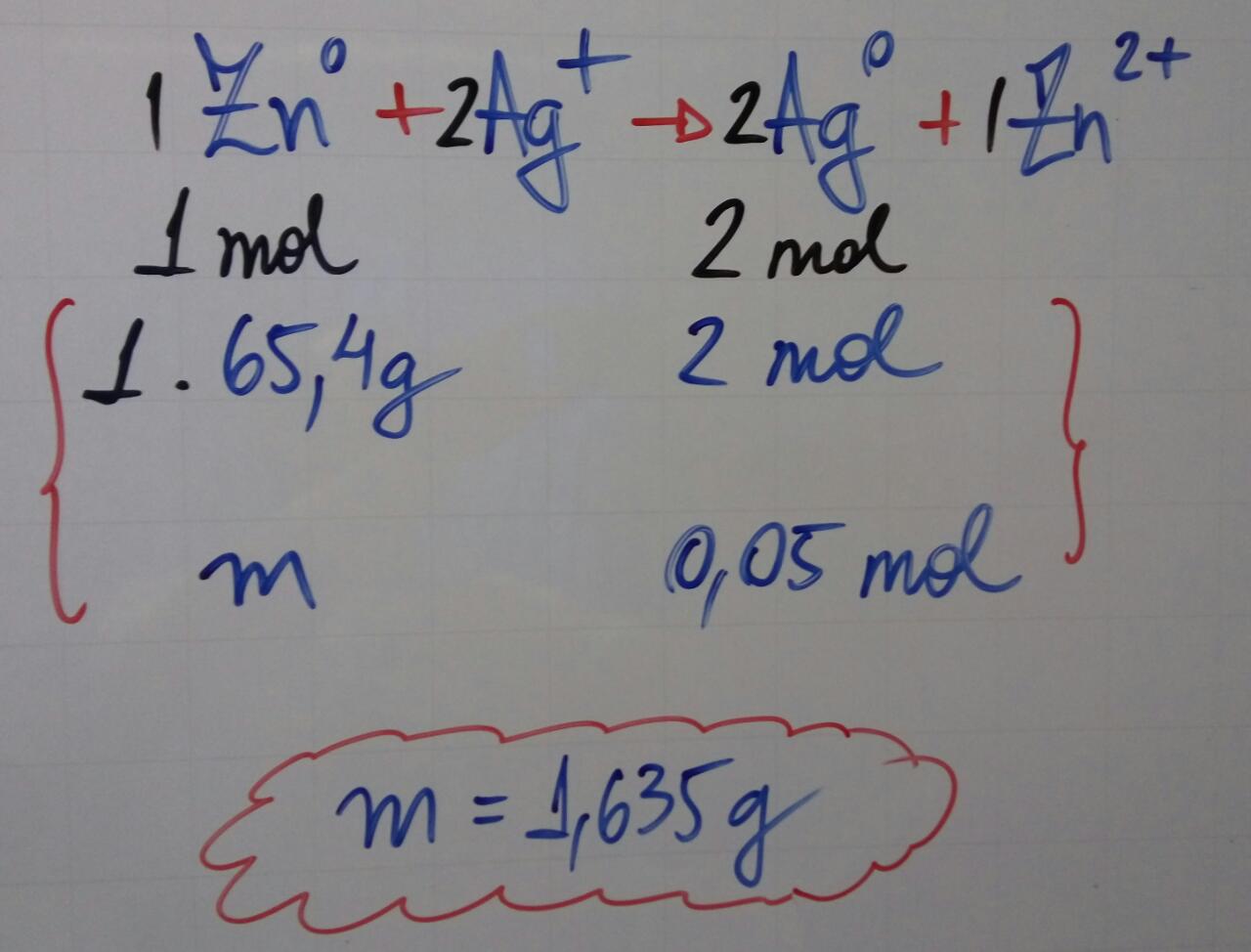
Jose Augusto
A diferença de potencial da pilha em condições-padrão (DEo) é igual à diferença entre o potencial-padrão da espécie que se reduz e o potencial-padrão da espécie que se oxida.
A espécie que se reduz é aquela de maior potencial-padrão de redução, no caso o íon Cu2+, e a espécie que se oxida é o Zno. Logo:
DEo = = + 0,34 – (– 0,76) = + 1,10 V
Na eletrólise, a massa de prata depositada no catodo corresponde a toda a massa de prata em solução e é calculada por:
108 g.mol–1 x 0,01 mol.L–1 x 0,5 L = 0,54 g
No anodo da pilha, ocorre a oxidação do zinco, representada pela semirreação:
Zno (s) Zn2+ (aq) + 2 e–
No catodo da eletrólise, ocorre a redução da prata, representada pela semirreação:
2 Ag+ (aq) + 2 e– 2 Ago (s)
Relacionando-se as semirreações, tem-se:
2 Ag+ (aq) + Zno (s) 2 Ago (s) + Zn2+ (aq)
Na eletrólise, a quantidade de matéria de prata depositada no catodo é calculada por:
0,01 mol.L–1 x 0,5 L = 0,005 mol Ag
A quantidade de matéria de zinco consumida é igual a:
2 x 0,005 mol = 0,0025 mol Zn
A massa de zinco correspondente é igual a:
0,025 mol x 65,5 g.mol–1 = 0,16375 g
Gabriel Carvalho
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 3 pág.
3 pág.



Compartilhar