Gnt alguem sabe me explicar por que o nitrogênio apresenta vários estado de oxidação diferente dos outros elementos do grupo 15?
💡 2 Respostas
Flávio Sousa
Todos os elementos do grupo do nitrogênio apresentam cinco elétrons na camada mais externa e o estado de oxidação máxima é +5, quando utilizam todos os elétrons para fazer ligações.
quando um átomo possui eletrons emparelhados a energia de ionização torna-se maior. É o chamado efeito do par inerte. Se a energia necessária para desemparelhar os elétrons for maior que a energia liberada na formação da ligação, então os elétrons permanecerão emparelhados.
o efeito do par inerte cresce com o aumento da massa atômica. Assim, geralmente só os elétrons p são utilizados, resultando uma valência 3.
Especialistas PD
Todos os elementos do grupo possuem cinco elétrons no nível eletrônico mais externo. Os estados de oxidação dos elementos desse grupo variam entre –3 a +5, sendo que o nitrogênio e o fósforo são encontrados em todos os estados possíveis de oxidação. Sua configuração da camada de valência é ns2np3.
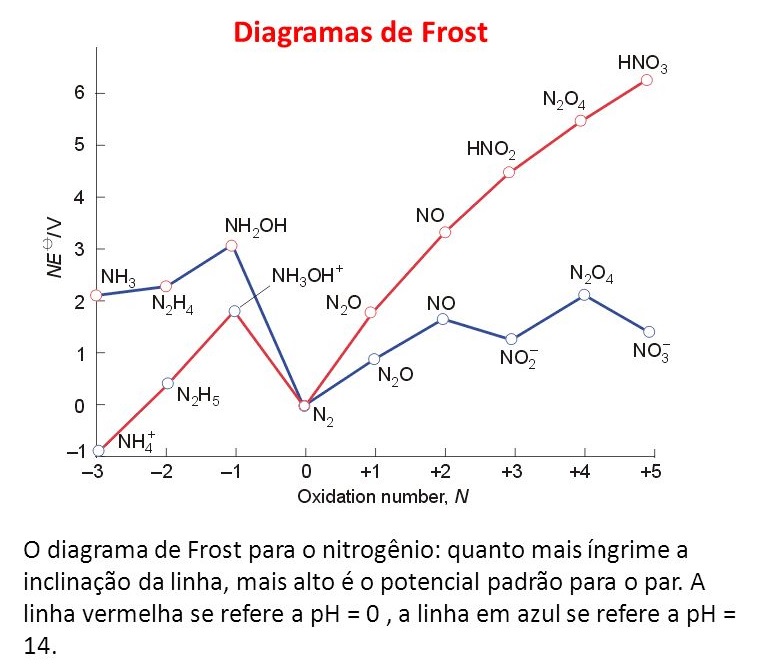
A química do nitrogênio é complexa. Para uma visão geral, considere o diagrama de estados de oxidação abaixo (Diagrama de Frost para o nitrogênio). Podemos notar que o nitrogênio pode assumir estados de oxidação formal que variam desde +5 até -3. Outra coisa, como ele se comporta de forma tão diferente em condições ácidas e básicas, assim podemos concluir que a estabilidade relativa de um estado de oxidação é muito dependente do pH.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Porque amônia não reage com metais no estado de oxidação zero
Química Inorgânica I
•UFMG
Thayline Coelho






Compartilhar