tirar duvidas
calcule o raio de um átomo de vanadio dado que o V possui uma estrutura cristalina C C C,uma massa especifica de 5,96 g/cm3, e o peso atômico de 50,9 g/mol
💡 3 Respostas
Carlos Alberto
d = densidade; m = massa; V = volume
d = m/V
5,96 = 50,9/V
V = 8,54027 cm^3
...................................................................................
Nós sabemos que 1 mol de átomos = 6,02 x 10^23 átomos
...................................................................................
O volume de um átomo de vanádio será então:
8,54027/6,02 x 10^23 = 1,419 x 10^-23 cm^3
...................................................................................
Considerando o átomo como uma esfera e sabendo que o volume (V) de uma esfera de raio (r) é dado por:
V = (4/3) x PI x r^3
1,419 x 10^-23 = (4/3) x PI x r^3
r = 1,5 x 10^-8 cm = 1,5 x 10^-10 m
Especialistas PD
Número de átomos em uma célula unitária na estrutura cristalina CCC (cúbica de corpo centrado): n = 2
densidade = 5,96 g/cm3
massa molar do vanádio: MM = 50,9 g/mol
constante de Avogadro: NA = 6,02 x 1023
massa de vanádio presente em uma célula unitária: m;
parâmetro de rede: a;
raio atômico: r.
O volume de uma célula unitária é: V = a3
Na estrutura CCC, temos que :
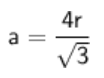
Logo, a fórmula do volume fica:
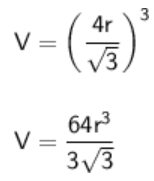
Pela fórmula da densidade, devemos ter
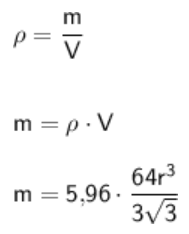
Montando a proporção entre as massas:
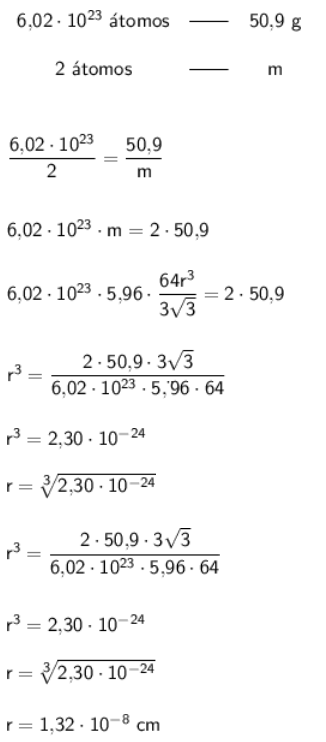
Sudomed Palmas Seguranca DO Trabalho
O sódio possui estrutura cristalina cúbica de corpo centrado, massa molar de 23 g mol-1 e massa especifica de 0,97 g cm-3.
Assinale a alternativa que apresenta o volume da célula unitária do sódio metálico.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar