Qual a forma predominante do aminoácido Histidina nos valores de pH 1,6 e 10?
💡 2 Respostas
RD Resoluções
Primeiramente, considere os valores de pKa para a Histidina:
\(pKa_1 = 1,82 \textrm{ (Grupo Carboxílico)}\)
\(pKa_R = 6 \textrm{ (Grupo R)}\)
\(pKa_2 = 9,7 \textrm{ (Grupo Amino)}\)
Lembre-se que, numa curva de titulação, todos os grupos ionizáveis encontram-se protonados quando \(pH < pKa_1\). Além disso, para cada valor de pKa, o respectivo grupo associado sofre desprotonamento, aumentando o pH do aminoácido. Dessa forma, todos os grupos ionizáveis encontram-se desprotonados quando \(pH > pKa_2\).
Veja que se \(pH = 1.6\) então \(pH < pKa_1\). Logo, todos os grupos ionizáveis estão protonados. Dessa forma, a forma predominante da histidina, neste caso, é a retratada abaixo:
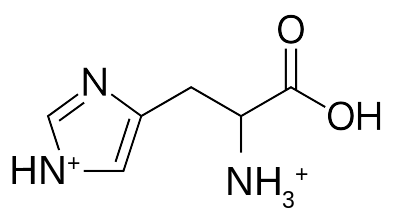
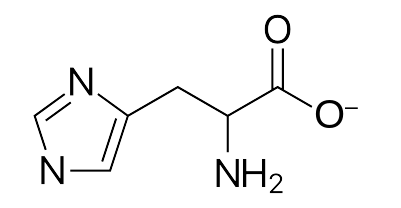
Agora, se \(pH = 10\) então \(pH > pKa_2\). Logo, todos os grupos ionizáveis estão desprotonados. Dessa forma, a forma predominante da histidina é:
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta








Compartilhar