Como calcular a carga líquida dos aminoácidos? a) Histidina em pH 12,0 b) Ácido glutâmico em pH 7,0 c) Prolina em pH 5,5
💡 5 Respostas
Andre Smaira
O pK é o valor de pH em que metade das moléculas está dissociada.
O ponto isoelétrico (pI) é o valor pH em que a carga elétrica é igual a zero.
----
Observe a tabela, que mostra os valores de pK e pI para os aminoácidos.
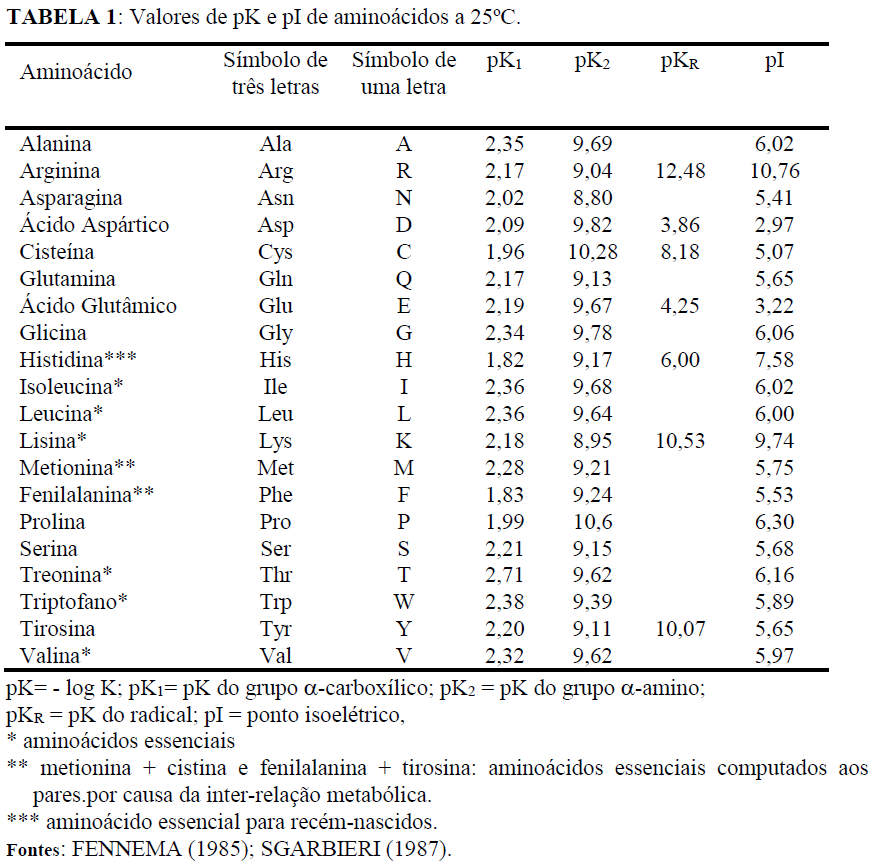
Tabela
-----
a) Histidina
Esse aminoácido possui \(p{K_1} = 1,82\), \(p{K_2} = 9,17\) e \(p{K_R} = 6,00\). Sabendo a estrutura desse aminoácido, podemos desenhá-lo e colocar suas devidas cargas em cada intervalo de \(pH\).
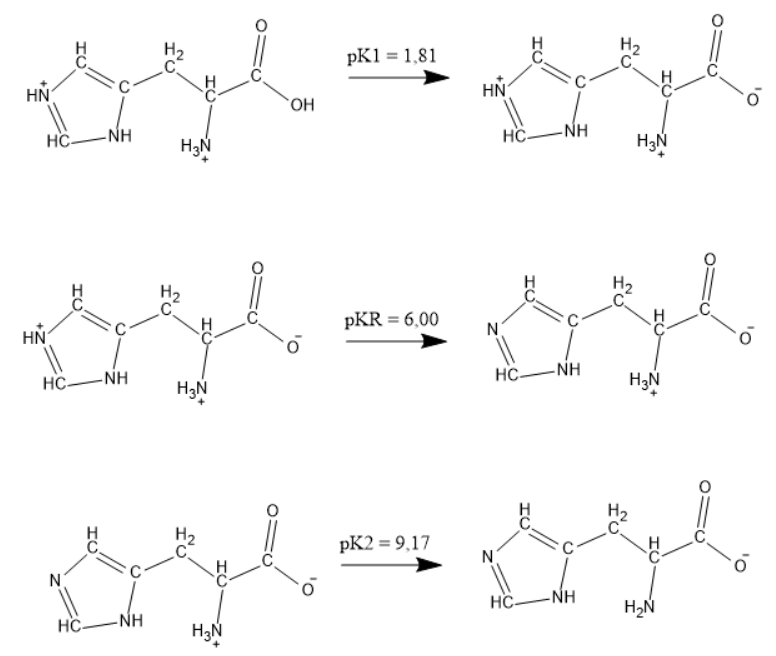
Histidina
Logo, em \(pH\) igual a \(12,0\) (que é maior que o valor de \(p{K_2}\)), temos que a carga líquida da histidina será de \(-1\).
------
b) Ácido glutâmico
Pela tabela, vemos que o ácido glutâmico possui \(p{K_1} = 2,19\), \(p{K_R} = 4,25\) e \(p{K_2} = 9,67\).
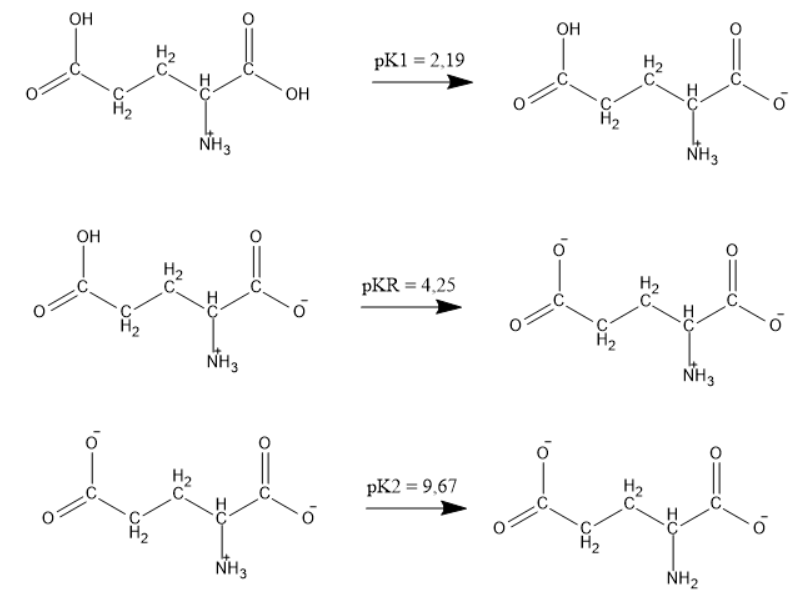
Ácido glutâmico
Em \(pH\) igual a \(7,0\) (entre os valores de \(p{K_R}\) e \(P{K_2}\)), a carga líquida do ácido glutâmico é \(-2\).
----
c) Prolina
Pela tabela, temos os valores \(p{K_1} = 1,99\) e \(p{K_2} = 10,6\).
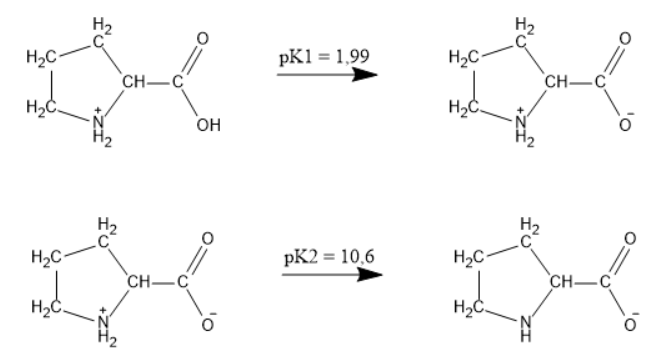
Prolina
Em \(pH\) igual a \(5,5\) (entre os valores de \(p{K_1}\) e \(p{K_2}\)), a carga líquida desse aminoácido é zero.
Temístocles Gomes
Quem souber me avisa tbm
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Qual a forma predominante do aminoácido Histidina nos valores de pH 1,6 e 10?
Bioquímica I
•ESTÁCIO EAD
gabriel frança






Compartilhar