Qual a diferença entre domínio de elétron ligante e um domínio de elétron não ligante?
💡 4 Respostas
Davi Lucas
adsadsssad
RD Resoluções
Um dos modos mais utilizados teoricamente para realizar a determinação da geometria molecular, ou seja, para descobrir a forma com que os átomos estão dispostos espacialmente em uma molécula, é pela teoria da repulsão dos pares eletrônicos, também conhecida como teoria da repulsão dos pares de elétrons da camada de valência (RPECV).
A geometria linear também ocorre no caso de moléculas que possuem três átomos e que o átomo central possui um de seus pares eletrônicos não compartilhado. É o caso do CS2. Vamos seguir os passos descritos para determinar a sua geometria.
1- Primeiro escrevemos a sua fórmula eletrônica de Lewis:
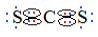
Fórmula eletrônica do CS2
2- Agora vamos determinar a quantidade de nuvens eletrônicas. Observe o carbono, que é o átomo central. Ele possui duas ligações duplas, então ele apresenta somente duas nuvens eletrônicas, cuja distância máxima possível forma um ângulo de 180ºC. Portanto, sua geometria é linear.
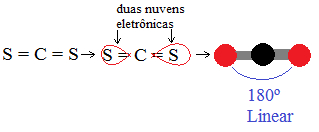
Geometria linear do CS2
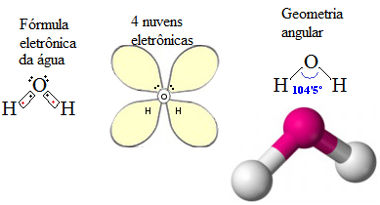
Mas existem casos de moléculas que possuem três átomos cuja geometria não é linear, mas sim angular. Isso acontece em moléculas que possuem um ou dois pares de elétrons desemparelhados. A água é um exemplo de molécula que possui geometria angular porque o átomo central (oxigênio) tem dois pares de elétrons não ligantes, conforme mostrado a seguir:
Thiago Paulino
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.






Compartilhar