Porque átomos com par de elétron não-ligante possui orbital P?
Dúvidas em Químicas
💡 3 Respostas
Jose Joaquim Raposo Neto
Lucas Renan Benincasa Pinheiro
RD Resoluções
Os orbitais são representados por nuvens eletrônicas e são diferentes para cada tipo de ligação; assim, para uma ligação do tipo s temos um orbital esférico; e para uma ligação p, temos um orbital na forma de duplo ovoide. Para o orbital de tipo p, há três possibilidades, pois existem três orientações espaciais possíveis (x, y, z). Considere a molécula de BeF2 (sabe-se experimentalmente que ela existe).
Vamos relembrar como ocorre o processo de hibridização
Relembrando: a hibridização é a “mistura” de orbitais atômicos puros, que originam orbitais atômicos híbridos equivalentes entre si, porém diferentes dos orbitais puros originais. Assim, isso ocorre nos orbitais do carbono que originalmente eram representados assim:
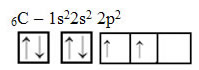
Porém, com o recebimento de energia, um elétron (representado por uma seta) do orbital 2s é promovido para o orbital 2p:
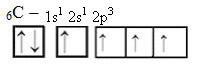
Dessa forma, o carbono fica com quatro orbitais desemparelhados, podendo realizar quatro ligações covalentes, não apenas duas.
No caso da hibridização do tipo sp, sabemos que duas ligações serão pi; essas ocorrem nos orbitais “p” puros, enquanto que os outros dois orbitais, que são híbridos do tipo sp, realizarão as ligações sigma restantes.
fonte:https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp.htm
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.




Compartilhar