Como calcular o numero de nox
Cr2O7-²
💡 3 Respostas
Raquel Nascimento
Aqui tem os metodos, flor: http://www.soq.com.br/conteudos/em/eletroquimica/p1.php
Zara Jardim
Obg gata !
Especialistas PD
Podemos seguir algumas regras para determinarmos o número de oxidação (Nox):
Regras para cálculo do Número de Oxidação (Nox):
1) H → maioria dos compostos Nox = +1.
Exceto se estiver ligado a metais, que são menos eletronegativos que ele, Nox = -1.
2) O → maioria dos compostos Nox = -2.
Exceto nos peróxidos (Nox = -1) e em floretos (Nox = +2 ou +1).
3) Metais Alcalinos (Família IA: Li, Na, K, Rb, Cs, Fr) Nox = +1.
4) Metais Alcainos Terrosos (Família IIA: Be, Mg, Ca, Sr, Ba) Nox = +2
6) Al → Nox +3
7) Zn → Nox +2
8) Substâncias Simples → Nox Zero
9) Íons monoatômicos → Nox = carga íon
10) Substâncias compostas → A soma dos nox dos elementos que compõem a substância é sempre zero.
11) Íons compostos → A soma dos Nox dos elementos que compõem o íon é sempre igual à sua carga.
Para o íon Cr2O7-2 temos:
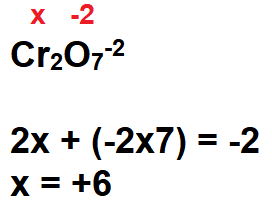
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
uma onda possui uma frequencia de 110rad/s eum comprimento de 1,8m, calcule o numero de onda
Física Geral e Experimental I
•FIC
Jose Ricardo
Como calcular a densidade através do coeficiente angular de uma curva de calibração?
Química Geral Experimental
•UNIFAL
Thaynan Bueno







Compartilhar