distribuição eletronica
Faça a distribuição eletrônica e a sua forma compacta, e dê os números quânticos do elétron mais energético e mais externo, especifique os números quânticos. Dê a localização do elemento na tabela e indique se são elementos representativos, de transição interna ou externa: Ni, Ni2+, Z= 14, 18, 53, 55, 64, 91, 5s2, 3p5. Determine o número atômico, o número máximo de elétrons, a designação do subnível e o número de orbitais em um átomo que podem ter: n=2 ms=-1/2; n= 5 l=3;n = 3 l = 2 ml = -1 ms = +1/2; n = 4 l = 1 ml = -1 ms = +1/2; n = 5 l = 1 ml = -1 ms = -1/2; n = 4 l = 2 ml = -3 ms = -1/2; n = 5 l = 0 ml = 0 ms = +1/2. Quantos valores possíveis existem para l e mlquando n=3 e n=5. Dê os valores para n, l e ml para cada orbital no subnível 2p, 3p, 2s, 4f, 5d, dê aquantidade de orbitais que existem em cada um desses subníveis.
💡 3 Respostas
Fabio Kuhn
dificil pergunta
Especialistas PD
Cada elétron de um átomo é caracterizado por quatro números quânticos:
- Número quântico principal: indica o nível ou camada do elétron
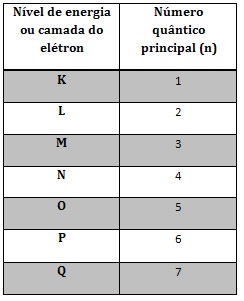
- Número quântico secundário: indica o subnível em que o elétron está
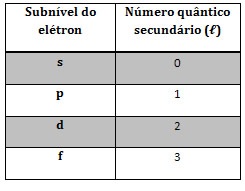
- Número quântico magnético: indica a orientação dos orbitais. Temos que distribuir os elétrons nas "caixinhas" que representam os orbitais. Ao preencher esses orbitais, deve-se seguir a Regra de Hund, que diz que isso deve ser feito de modo que tenhamos o maior número possível de elétrons desemparelhados, isto é, isolados. Isso significa que preenchemos todas as setas para cima e só depois voltamos preenchendo com as setas para baixo.
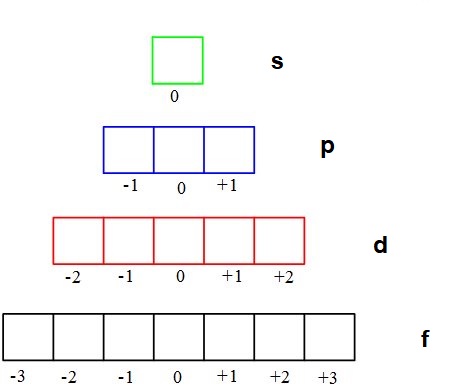
- Número quântico spin: mostra o sentido da rotação do elétron. Se o orbital de um subnível for negativo, a rotação é no sentido negativo, o qual é representado por uma seta para cima. Mas, se o orbital de um subnível for positivo, a rotação é no sentido positivo, o qual é representado por uma seta para baixo. Então seta pra cima: - 1/2. Seta para baixo: + 1/2.
Por exemplo:
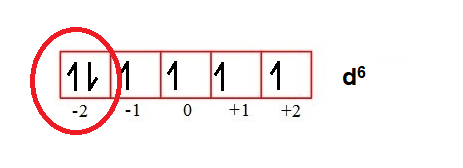
Distribuição eletrônica do ferro: 1s2 2s2 2p6 3s2 3p6 4s2 3d6
- Tendo em conta que o seu elétron mais energético se encontra na camada 3, então, n = 3.
- Seu subnível é d, então, l = 2.
- O subnível d possui 5 órbitas. Ao distribuir os elétrons, o último fica no orbital -2, então, m = -2.
- O spin +½
Lena Ramos
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
,Qual a distribuição eletronica do ion de Hidrogenio?
Laboratório de Física e Química
•DOM BOSCO
Neneiin Santtos
Materiais relacionados
 3 pág.
3 pág.



Compartilhar