Uma determinada substância pode ser solúvel em solventes com polaridades diferentes como água e hexane?
💡 3 Respostas
Caio Menezes
Muitas substâncias conseguem ser solúveis tanto em solventes polares quanto em apolares, o que muda é o grau de solubilidade. Neste caso, ele está ligado com as forças intermoleculares entre as moléculas do soluto e do solvente (mais diretamente com a simetria das moléculas, a diferença de eletronegatividade e a densidade eletrônica, além da concentração).
Exemplos desses casos:
Iodo - muito solúvel em benzeno e muito pouco (mas solúvel) em água;
Sabões - solúvel em água e óleo (formação de miscelas);
Álcool - é solúvel tanto em gasolina (desde que seja anidro) quanto em água.
Acetona - solúvel em muitos solventes apolares e polares.
Material para leitura:
http://www.mundoeducacao.com/quimica/moleculas-organicas-polares-apolares.htm
http://www.brasilescola.com/quimica/relacao-entre-forca-intermolecular-solubilidade-das-substancias.htm
Pablo Radific
Cara acho que sim, por exemplo alguns compostos orgânicos tem cadeias grandes com uma parte polar e outra apolar sendo assim possivel ser solúvel em solventes com polaridades diferentes, sendo mais soluvel em um solvente do que em outro.
Especialistas PD
Existem três aspectos que devem ser considerados quando analisamos a solubilidade dos compostos orgânicos em água e entre si, que são: a polaridade, as forças de atração intermolecular e o tamanho da cadeia carbônica.
Polaridade: Há uma regra (que está sujeita a exceções) que se aplica não somente aos compostos orgânicos, mas à grande maioria das substâncias, no que se refere à solubilidade, que é: semelhante dissolve semelhante. Ou seja, substância polar é solúvel em solvente polar e substância apolar é solúvel em solvente apolar.
Forças de atração intermolecular: Embora os solutos apolares se dissolvam melhor em solventes apolares e vice-versa, existem exceções, como ocorre com a gasolina, que é apolar e se dissolve muito bem no etanol, que é polar. Assim, o mais correto é considerar a solubilidade em termos de intensidade das forças intermoleculares. A possibilidade de ocorrer a dissolução aumenta quando a intensidade das forças atrativas entre as moléculas de soluto e de solvente é maior ou igual à intensidade das forças de atração entre as moléculas do próprio soluto e entre as moléculas do próprio solvente.
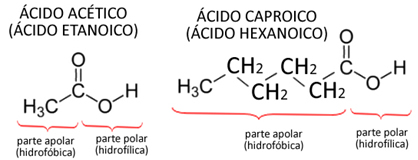
Tamanho das cadeias carbônicas: Além da semelhança de polaridade e das interações intermoleculares, o tamanho aproximado das moléculas também contribui para uma maior solubilidade. Por exemplo, isso é verificado quando consideramos o ácido acético, cuja estrutura está representada a seguir. Este composto é solúvel em água em quaisquer proporções porque, o ácido acético possui uma parte hidrofílica, que tem afinidade com a água, que é a extremidade com o grupo OH; mas também possui uma parte hidrofóbica, que não tem afinidade com a água, que é a cadeia carbônica. Já o ácido caproico, mostrado ao lado da estrutura do ácido acético, é parcialmente solúvel em água. Isso ocorre porque sua parte hidrofóbica é maior.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Uma determinada substância pode ser solúvel em solventes com polaridades diferentes como água e hexano?
Química Geral e Inorgânica
•UNISOCIESC
Dyonata Florencio
Para preparar uma solução estoque a partir de um padrão, é mais aconselhável usar uma pipeta volumétrica ou graduada?
Química Geral Experimental
•USP-RP
Felipe Forense
Segundo a legislação, qual é a quantidade máxima de etanol anidro que pode ser adicionado à gasolina?
Química Geral Experimental
•USP-RP
Felipe Forense
Materiais relacionados
 7 pág.
7 pág. 3 pág.
3 pág.




Compartilhar