Quais são as principais características das funções orgânicas ??
Álcool, Fenol, Amida, Ácido Carboxílico, Éster, Cetona, Éter são algumas funções orgânicas são funções orgânicas , mas quais são suas características ? Como podemos diferencialo-los quanto ao seu uso ?
💡 4 Respostas
Daniel Bispo
Espero que esta tabelinha te ajude...
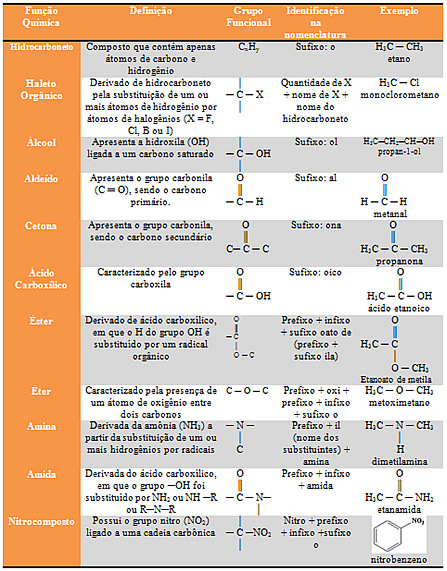
Att,
Daniel Bispo.
Mariana Tôrres de Castro
Alcoóis - compreendem uma grande família de compostos orgânicos que possuem uma hidroxila (OH) ligada a um carbono saturado (sp3 ). As ligações C-O e O-H são polares, e isso responde grande parte pela reatividade dos alcoóis. Além disso, o hidrogênio ligado ao oxigênio faz ligação hidrogênio – força intermolecular forte –, o que faz, por exemplo, com que não existam alcoóis gasosos nas condições normais de temperatura e pressão (CNTP). Os alcoóis sofrem vários tipos de reações. Como o oxigênio é muito eletronegativo, o hidrogênio da hidroxila é ácido. Podemos também retirar o hidrogênio por reação clássica ácido-base, mas aí temos de usar bases muito fortes, pois os alcoóis são ácidos fracos. Como o oxigênio possui dois pares de elétrons não ligantes (conte o número de elétrons em torno do oxigênio e repare que para completar o octeto existem quatro elétrons que não estão fazendo ligação) eles podem receber um H+, ou seja, também podem atuar como base. Os cátions resultantes dessa reação são chamados de íons alquil-oxônios e são muito utilizados como intermediários em reações de substituição e eliminação de alcoóis (para aumentar a reatividade dos alcoóis). Substâncias que podem atuar tanto como bases quanto como ácidos são denominadas anfotéricas. Como os alcoóis primários (RCH2OH) possuem dois hidrogênios ligados ao carbono em que está ligada a hidroxila, sofrem oxidação parcial até aldeído (só um hidrogênio é oxidado) ou total (oxidação dos dois hidrogênios) até ácido carboxílico. Os alcoóis secundários (R2CHOH) são oxidados a cetonas. Alcoóis terciários, como não possuem hidrogênio ligado ao carbono que contém hidroxila não são oxidados.
Fenóis - são uma classe de compostos orgânicos que possuem a hidroxila diretamente ligada a um anel aromático. Os fenóis são bem mais ácidos que os alcoóis porque o sal resultante (fenolato ou fenóxido) é estabilizado por ressonância. Assim, pode-se usar bases mais fracas, como NaOH ou KOH (essas bases não reagem com alcoóis). Esses fenolatos são muito reativos e utilizados para a síntese de éteres alquil-arílicos. Os fenóis não reagem como base – pelo mesmo motivo que explica a sua acidez: como os pares de elétrons do oxigênio (um de cada vez) estão deslocalizados pelo anel aromático não estão disponíveis para se ligar ao hidrogênio, pois perderiam essa capacidade de deslocalização. Essa diferença de caráter básico é evidenciada em uma reação clássica para a formação de ésteres a esterificação de Fischer. os fenóis não formam ésteres aromáticos por reação com ácidos carboxílicos (porque não têm o caráter básico dos alcoóis). Os fenóis também sofrem reações de substituição no anel aromático, no qual o hidrogênio ligado ao anel é substituído por um átomo ou grupo de átomos. Da mesma forma que os halogênios, as substituições sempre ocorrem nas posições orto e para em relação à hidroxila fenólica.
Éteres - Quando o hidrogênio da OH de alcoóis e fenóis é substituído por um grupo alquil ou aril, temos a classe dos éteres. Os éteres são pouco reativos (só sofrem basicamente reações de clivagem-quebra - por ácidos) e por causa dessa propriedade são muito usados como solventes (um solvente só deve dissolver as substâncias, e não reagir com elas. Aí seria um reagente!).
Aldeídos e cetonas - possuem como grupo funcional a carbonila, no qual o carbono está hibridizado sp2. Essa ligação é polar – o carbono está com caráter positivo: eletrofílico – e é a responsável pela grande reatividade dessa classe de compostos. Os aldeídos e cetonas com pelo menos um hidrogênio α (hidrogênio ligado no carbono vizinho ao grupo carbonila) encontram-se em um equilíbrio dinâmico com um isômero denominado enol. Esse equilíbrio é denominado tautomerismo cetoenólico e, na grande maioria das vezes, está deslocado sempre para a forma ceto (para os aldeídos ou cetonas), isto é, sempre tem muito mais aldeído ou cetona do que enol. Aldeídos e cetonas são muito usados em perfumaria e indústrias alimentícias e farmacêuticas como odorizantes.
Os aldeídos e cetonas são muito importantes na Química Orgânica devido à versatilidade, ao grande número de reações de que podem participar, com possibilidade de formação de vários tipos de produtos. Observando as características do grupo funcional carbonila para o qual a gente estende essa reatividade: como contém uma insaturação (C=O), apresentam, por isso, tendência a sofrer reações de adição, como os alcenos. Todavia, diferentemente dos alcenos, a ligação é muito polarizada, o que traz consequências importantes. O carbono tem caráter positivo e assim sofre ataque de espécies que possuem uma carga negativa ou um par de elétrons não ligantes (nucleófilos). Lembre que nos alcenos quem inicia a reação de adição à C=C é uma espécie positiva – um eletrófilo.
A reação de Grignard é um exemplo clássico de adição nucleofílica à carbonila. Como no reagente de Grignard, o carbono está ligado a um metal – mais eletropositivo – o carbono está com caráter nucleofílico e então se adiciona à carbonila, formando alcoóis. Observe – analise as estruturas – que reações com o formaldeído sempre formam alcoóis primários, com aldeídos são formados álcoois secundários e com cetonas, alcoóis terciários. Como o hidrogênio é menor que grupos alquila, em todas as reações de adição nucleofílica os aldeídos reagem mais rapidamente que as cetonas (tem mais espaço para o nucleófilo atacar a carbonila de aldeídos) e o formaldeído é o mais reativo de todos (tem hidrogênio dos dois lados). Outra reação de adição nucleofílica à C=O, e que acontece muito na natureza, é a da adição de alcoóis a aldeídos, formando hemiacetais e acetais (ou hemicetais ou cetais, se ocorrer com cetonas).
Essas funções orgânicas são muito instáveis – porque contêm dois átomos de oxigênio eletronegativos ligados a um mesmo carbono e normalmente a gente não consegue obtê-los (rapidamente voltam para as cetonas ou aldeídos, embora esteja comprovado que se formam!). Todavia, quando as funções OH e C=O estão na mesma molécula, essa reação acontece bem mais facilmente e os produtos são, também, facilmente isolados.
Além da reação de adição à carbonila, os aldeídos podem sofrer reações de oxidação, formando ácidos carboxílicos – existem inúmeros reagentes que podem fazer isso. Aldeídos e cetonas podem ser reduzidos, e aí, dependendo do reagente usado, vão formar alcoóis.
Ácidos carboxílicos - possuem como grupo funcional a carboxila: COOH. Comparados com os demais compostos orgânicos, são ácidos mais fortes. Devido ao seu caráter ácido, os ácidos carboxílicos sofrem reações de neutralização com bases formando sais. Os ácidos carboxílicos sofrem principalmente reações de substituição da OH por outros átomos ou grupos de átomos que são denominadas de reações de substituição no grupo acila (acila é o nome de radicais do tipo RCO). Essas reações formam compostos constituintes de uma grande variedade de classes funcionais, chamadas genericamente de derivados dos ácidos carboxílicos, que são: haletos de ácidos, anidridos, ésteres, amidas e nitrilas.
Ésteres - nos ésteres, o hidrogênio da carboxila (COOH) dos ácidos carboxílicos é substituído por um grupo alcolato (OR ou OAr). Os ésteres cíclicos recebem a designação de lactonas. Os ésteres têm várias aplicações: como solventes, polímeros (poliésteres), medicamentos, flavorizantes e na fabricação de sabões. A hidrólise de ésteres em meio ácido forma ácido carboxílico e álcool (é o reverso da esterificação de Fischer) e, em meio básico, forma os sais de ácidos carboxílicos (carboxilatos) e álcool. Essa hidrólise é denominada de saponificação, pois é a reação que produz sabão. Os ésteres sofrem também reações de transesterificação (troca do grupo alcolato). Esse tipo de reação é usado na preparação do biodiesel, que é uma reação de transesterificação: o alcolato (glicerol) dos óleos vegetais é substituído por metoxilato. Os ésteres também reagem com aminas, formando amidas (reações de amonólise – quando o reagente é a amônia – e aminólise – reação com outras aminas). Os ésteres (bem como os cloretos de ácido, anidridos e nitrilas) reagem com os reagentes de Grignard formando alcoóis terciários.
Amidas - são derivados de ácidos carboxílicos em que a hidroxila é substituída por amônia ou aminas (RCONH2, RCONHR, RCONR2). As amidas cíclicas são denominadas lactamas. Da mesma forma que as aminas são classificadas em primárias, secundárias ou terciárias em função do número de substituintes que existem no nitrogênio. As amidas têm grande aplicação como polímeros, exemplos são os náilons (nome genérico dado para as poliamidas) e os poliuretanos, como medicamentos, herbicidas, repelentes de insetos, dentre outras várias aplicações. A ligação amídica (NH-C=O) é importantíssima para os seres vivos. Para formar os peptídeos (e, daí, as proteínas) os aminoácidos – como o nome já diz, são compostos polifuncionais que possuem pelo menos uma função amina e uma carboxila – ligam-se uns aos outros pelas chamadas ligações peptídicas: uma amida. Os peptídeos e as proteínas são, portanto, poliamidas. As amidas são os derivados de ácidos carboxílicos menos reativos. Para serem hidrolisadas até ácidos carboxílicos – lembrem-se que a definição de derivado de ácido carboxílico é: todo composto que por hidrólise forma ácido carboxílico – exigem longo tempo de aquecimento e uso de ácidos minerais como catalisadores.
Eduardo Kaiser Buffon
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta







Compartilhar