Misturam-se 2 mols de ácido acético com 3 mols de álcool etílico, a 25°C, e espera-se atingir o equilíbrio.
Sendo o valor de Kc, a 25°C, igual a 4, as quantidades aproximadas, em mols, de ácido acético e acetato de etila são, respectivamente:
A - 2 e 5
B - 3,57 e 4,57
C - 0,43 e 1,57
D - 3,57 e 1,57
💡 6 Respostas
Andre Smaira
prática nosso conhecimento sobre Química.
----
A constante de equilíbrio (Kc) é o valor relacionado a concentração dos reagentes e do produto no momento do equilíbrio, isso só acontece em reações reversíveis.
A fórmula da constante de equilíbrio é:
\[{{\rm{k}}_c}{\rm{ = }}{{\left[ {{\rm{produto}}} \right]} \over {\left[ {{\rm{reagente}}} \right]}}\]
Sendo que os coeficientes são apresentados da seguinte maneira:
\[{\rm{aB + cD }} \mathbin{\lower.3ex\hbox{\$\buildrel\textstyle\rightarrow\over {\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}\$}} {\rm{ eF + gH}}\]
\[{{\rm{k}}_c}{\rm{ = }}{{{{\left[ {\rm{F}} \right]}^{\rm{e}}}{{\left[ {\rm{H}} \right]}^{\rm{g}}}} \over {{{\left[ {\rm{B}} \right]}^{\rm{a}}}{{\left[ {\rm{D}} \right]}^{\rm{c}}}}}\]
Um exemplo de fórmula de calcular o Kc é a seguinte:
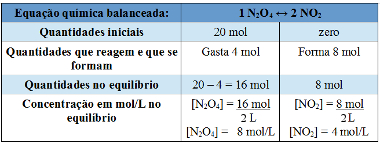
Exemplo de Tabela usada para resolver Kc
Em uma mistura com 2 mols de ácido acético e 3 mols de álcool etílico, a 25°C, com Kc = 4, temos a seguinte resolução.
\[\eqalign{ & 4{\rm{ = }}{{{\rm{a x a}}} \over {\left( {{\rm{2 - a}}} \right){\rm{ }}\left( {{\rm{3 - a}}} \right)}} \cr & 4{\rm{ = }}{{{{\rm{a}}^2}} \over {{{\rm{a}}^{\rm{2}}}{\rm{ - 5a + 6}}}} \cr & {\rm{4}}\left( {{{\rm{a}}^{\rm{2}}}{\rm{ - 5a + 6}}} \right){\rm{ = }}{{\rm{a}}^{\rm{2}}} \cr & 4{{\rm{a}}^{\rm{2}}}{\rm{ - 20a + 24 - }}{{\rm{a}}^{\rm{2}}}{\rm{ = 0}} \cr & {\rm{3}}{{\rm{a}}^2}{\rm{ - 20a + 24 = 0}} }\]
Agora basta calcular a raiz da equação:
\[\eqalign{ & {\rm{a = }}{{ - b \pm \sqrt {{b^2} - 4ac} } \over {2a}} \cr & {{\rm{a}}_2}{\rm{ = }}{{{\rm{ - }}\left( { - 20} \right){\rm{ - }}\sqrt { - {{20}^2} - 4{\rm{ x 3 x 24}}} } \over {2{\rm{ x 3}}}} \cr & {{\rm{a}}_1}{\rm{ = }}{{{\rm{ 20 - }}\sqrt {400{\rm{ - 288}}} } \over 6} \cr & {{\rm{a}}_1}{\rm{ = }}{{{\rm{ 9}}{\rm{,41}}} \over 6} \cr & {{\rm{a}}_1}{\rm{ = 1}}{\rm{,57}} }\]
\[\eqalign{ & {{\rm{a}}_2}{\rm{ = }}{{{\rm{ - }}\left( { - 20} \right){\rm{ + }}\sqrt { - {{20}^2} - 4{\rm{ x 3 x 24}}} } \over {2{\rm{ x 3}}}} \cr & {{\rm{a}}_2}{\rm{ = }}{{{\rm{20 + }}\sqrt {400{\rm{ - 288}}} } \over 6} \cr & {{\rm{a}}_2}{\rm{ = }}{{{\rm{30}}{\rm{,58}}} \over 6} \cr & {{\rm{a}}_2}{\rm{ = 5}}{\rm{,09}} }\]
Porém a única que satisfaz o problema é 1,57 que é o valor de acetato de etila. Já para o Ácido acético basta calcular:
Ácido acético
\[2 - 1,57 = 0,43\]
---
Portanto a alternativa correta é a letra c.
Rodrigo RfrZz
letra C
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar