Calcular a força iônica dos seguintes eletrólitos: (a) NaCl 0,2 mol/kg; (b) CaCl2 0,2 mol/kg; (c) NaCl 0,1 mol/kg + CaCl2 0,1 mol/kg.
💡 4 Respostas
Diogo Dias
A força íonica é dada por Fi =\(\sum_{i=1}^{N} n_ic_iz_i^2\) onde N é o número total de espécies,ni é a quantidade de espécie dissociada (CaCl2 nCa=1 e nCl=2) , ci é a concentração de cada uma das espécies e zi é a carga da espécie.
Um exemplo:
Uma solução de NaCl a 0,001molL-1 , possui z=+1 para o sódio e z=-1 pra o cloreto, a força iônica desta solução é 1/2(0,001x(+1)²+0,001x(-1)²)=0,001molL-1.
com base no exemplo, temos para (a) Fi=0,2 molL-1;(b) Fi=1/2(0,2x(+2)²x2x0,2x(-1)² )molL-1=0,6molL-1; (c) (b) Fi=1/2(0,1x(+1)²+0,1x(+2)²+3x0,1x(-1)² )molL-1=0,4molL-1
Espero ter judado.
Especialistas PD
A formação de pares iônicos é decorrente da ação de forças eletrostáticas de todas as espécies eletricamente carregadas em solução, os íons, que devem afetar a atividade de uma espécie em particular presente nessa mesma solução. Para expressar essa característica da solução, em essência seu “conteúdo” em íons, existe o parâmetro denominado força iônica, μ:
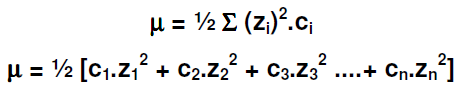
em que ci é a concentração analítica de cada íon presente em solução e zi sua carga. A força iônica é uma medida do potencial elétrico da solução e não tem unidade.
- NaCl 0,2 mol/kg
NaCl → Na+ + Cl-
μ = 1/2 . ([Na+] . Z[Na+]2) + ([Cl-] . Z[Cl-]2)
μ = 1/2 . (0,2.12) + (0,2 . -12) = 0,2
- CaCl2 0,2 mol/kg
CaCl2 → Ca2+ + 2 Cl-
μ = 1/2 . (0,2.22) + (2.0,2.12) = 0,6
- NaCl 0,1 mol/kg + CaCl2 0,1 mol/kg
μ = 0,4
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 9 pág.
9 pág. 7 pág.
7 pág.





Compartilhar