UERJ 2012 - O monóxido de carbono, formado na combustão incompleta em motores automotivos, é um gás extremamente tóxico.
fim de reduzir sua descarga na atmosfera, as fábricas de automóveis passaram a instalar catalisadores contendo metais de transição, como o níquel, na saída dos motores.
Observe a equação química que descreve o processo de degradação catalítica do monóxido de carbono:
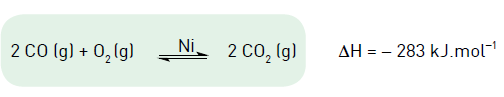
Com o objetivo de deslocar o equilíbrio dessa reação, visando a intensificar a degradação
catalítica do monóxido de carbono, a alteração mais eficiente é:
(A) reduzir a quantidade de catalisador
(B) reduzir a concentração de oxigênio
(C) aumentar a temperatura
(D) aumentar a pressão
💡 2 Respostas
Camila Assis
O objetivo é deslocarmos o equilíbrio da reação de degradação catalítica do monóxido de carbono para a direita, sentido direto de formação dos produtos, onde intensificaremos a degradação!
Se reduzirmos a quantidade de catalisador (alternativa a), a reação ficaria mais lenta. Se a concentração de oxigênio fosse reduzida (alternativa b), o equilíbrio se deslocaria para o sentido inverso, para compensar essa perda de reagente. Se aumentamos a temperatura dessa reação (alternativa c), que é uma reação exotérmica (libera calor, variação de entalpia negativa), o equilíbrio se desloca para o sentido dos reagentes.
Se aumentarmos a pressão (alternativa d), o equilíbrio se deslocará no sentido de menor volume (mols gasosos), de acordo com o princípio de Le Chatelier. Temos nessa reação 3 mols gasosos nos reagentes e apenas 2 nos produtos, então o equilíbrio se deslocará para o sentido direto, intensificando a degradação!
Gabarito: letra D
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 1 pág.
1 pág. 1 pág.
1 pág.




Compartilhar