Uerj 2017 - Indicadores ácido-base são substâncias que, ao serem adicionadas a soluções aquosas,
modificam sua coloração de acordo com o pH do meio. Observe a seguir a variação de cor proporcionada por quatro indicadores em função do pH.
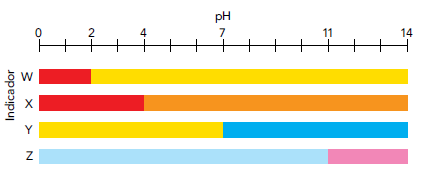
Considere o preparo em laboratório de duas soluções aquosas de NaOH com concentrações de 10−2 mol.L-1 e 10−6 mol.L-1, a 25 ºC.
É possível diferenciar visualmente essas soluções com a adição do seguinte indicador:
(A) W
(B) X
(C) Y
(D) Z
💡 3 Respostas
Camila Assis
Para escolhermos qual indicador será usado, primeiro vamos determinar o pH (a figura está em pH) das duas soluções aquosas de NaOH. Como se trata de uma base forte, temos:
pOH = - log [OH-]
pH + pOH = 14
1ª solução:
pOH = - log [10-2] = 2
pH = 12
2ª solução:
pOH = - log [10-6] = 6
pH = 8
Então temos que escolher um indicador que apresentará coloração diferente em pH 12 e 8, que é o indicador Z. Ele apresenta coloração rosa no pH = 12 e coloração azul no pH = 8.
Gabarito: letra D
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar