(ITA 2017) Gás cloro é borbulhado em uma solução aquosa concentrada de NaOH a quente, obtendo-se dois ânions X e Y.
a) Quais são estas espécies X e Y?
b) Com a adição de solução aquosa de nitrato de prata poder-se-ia identificar estes ânions? Justifique sua resposta utilizando equações químicas e descrevendo as características do(s) produto(s) formado(s).
💡 2 Respostas
Educador e Engenheiro
Caros alunos,
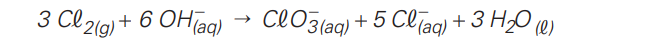
Subtende-se que a solução está acima de 40 ° C (quente!), logo há formação de clorato no lugar do ânion do hipoclorito (ClO-).
Adicionando o nitrato de prata, sucederá uma dissociação química (Ag+ e NO3-) com subsequente formação de precipitado (o cátion de prata com o ânion do cloro) , conforme reação abaixo:
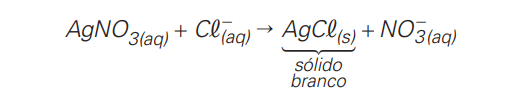
Bons estudos e um abraço fraterno,
Camila Assis
Quando borbulhamos gás cloro em uma solução de hidróxido de sódio, temos a reação balanceada:
3 Cl2 + 6 NaOH → 5 NaCl + NaClO3 + 3 H2O
a) Os ânions obtidos são o cloreto, Cl- e o clorato, ClO3-.
NaCl → Na+ + Cl-
NaClO3 → Na+ + ClO3-
b) Ao adicionarmos nitrato de prata, AgNO3, podemos identificar o íon cloreto, já que reagirá com Ag+ e precipitará na forma de cloreto de prata, AgCl. Já o íon clorato não precipita.
Ag+ + Cl- → AgCl
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 28 pág.
28 pág.




Compartilhar