(ITA 2017) Considere as substâncias o-diclorobenzeno e p-diclorobenzeno.
a) Escreva as fórmulas estruturais de ambas as substâncias.
b) Para ambas as substâncias, forneça um nome sistemático diferente daquele informado no enunciado.
c) Qual das duas substâncias tem maior ponto de ebulição? Justifique sua resposta.
💡 3 Respostas
Educador e Engenheiro
Caro aluno,
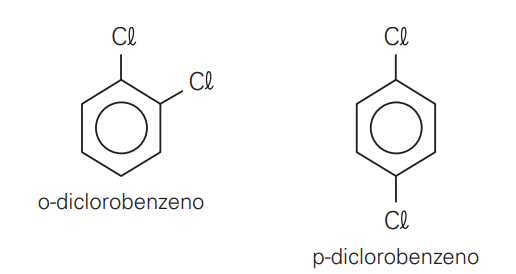
Conforme explanado acima, o (o-diclorobenzeno) pode ser chamado de 1,2-diclorobenzeno. (devido a posição do cloro), ao passo que o (p-diclorobenzeno) pode ser o 1,4 - diclorobenzeno. O maior ponto de ebulição, por sua vez, será associado ao tipo de ligação intermolecular que cada composto fará. Por conseguinte, como pode ser observado, o-diclorobenzeno possuirá maior ponto de ebulição (é uma molécula POLAR) - momento resultante diferente de 0. O p-diclorobenzeno apresenta os seus cloros em posição de para, isto é, em uma mesma direção (vertical), porém em sentidos opostos. Lembre-se que o elemento mais eletronegativo tende a puxar a nuvem de elétrons; portanto, o vetor parte do CARBONO em direção ao CLORO e então são cancelados. Com efeito, o p-diclorobenzeno terá o momento resultante igual a 0!!! (APOLAR!!!)
Estudante PD
a) Fórmulas estruturais exigidas:
p-diclorobenzeno:
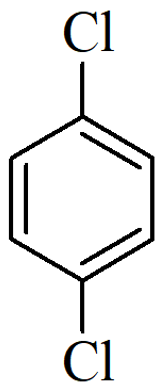
o-diclorobenzeno:
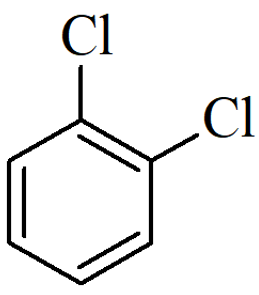
b) Nomes sitemáticos:
p-diclorobenzeno = 1,4-diclorobenzeno
o-diclorobenzeno = 1,2-diclorobenzeno
c) Comparativo entre os pontos de ebulição:
o-diclorobenzeno = composto polar (força intermolecular do tipo dipolo-dipolo).
p-diclorobenzeno = composto apolar (força do tipo dipolo intântaneo induzido).
Em termos de força:
força intermolecular do tipo dipolo-dipolo > força do tipo dipolo intântaneo induzido
Logo, o ponto de ebulição do o-diclorobenzeno é maior que o ponto de ebulição do p-diclorobenzeno.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta







Compartilhar