Como seria a resolução desse exercício?????
O cloreto de cálcio (CaCl2) é um sólido higroscópico, ou seja, que absorve facilmente a umidade do ambiente em que se encontra. Devido a essa característica, tem grande aplicação na composição da salmoura para sistemas de refrigeração e em produtos antimofos.
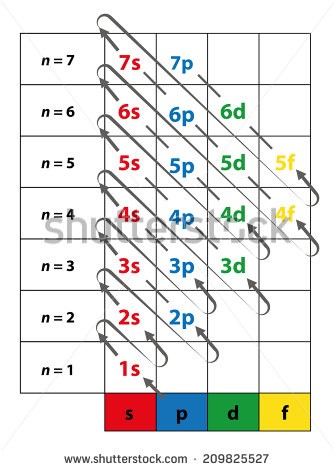
O cloreto de cálcio é resultado da ligação entre os elementos Ca e Cl, cujos números atômicos são, respectivamente, 20 e 17. Com base no diagrama de Linus Pauling, descreva a configuração eletrônica desses elementos e explique que tipo de ligação química realizam entre eles. Explique como este tipo de ligação funciona.
💡 1 Resposta
João Guaripuna
Através da distribuição eletrônica e análise da tabela periódica podemos prever o tipo de ligação que os elementos podem fazer.
Distribuição eletrônica do cálcio (Ca) e do cloro (Cl):
Cálcio (₂₀Ca): 1s² 2s² 2p⁶ 3s² 3p⁶ 4s²
Cloro (₁₇Cl): 1s² 2s² 2p⁶ 3s² 3p⁵
O átomo de cálcio irá doar os dois elétrons da camada de valência formando o cátion Ca²⁺. Já o átomo de cloro irá receber um elétron formando o íon Cl⁻.
Composto formado:
Ca²⁺ + Cl⁻ ⇒ CaCl₂
A ligação que ocorre entre os átomos neste composto é do tipo iônica, pois temos uma transferência de elétrons.
Metal + ametal ou metal + hidrogênio ⇒ ligação iônica
Leia mais em Brainly.com.br - https://brainly.com.br/tarefa/29875279#readmore
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
AV1 - Atividade Contextualizada Conteúdo do exercício
Laboratório de Química Geral e Inorgânica
•UNINTER
silvania.vitoria







Compartilhar