qual é a relaçao entre o grafico de Michaelis-Menten e o de Lineweaver- Burk?
💡 2 Respostas
Estudante PD
O gráfico de velocidade face a [S] mostrado anteriormente não é linear(grafico de Michaelis-Menten). Embora a baixas concentrações de substrato se mantenha linear, vai curvando à medida que aumenta a concentração de substrato. Antes da chegada dos computadores, que permitem ajustarregressões não lineares de forma simples, podia chegar a ser realmente difícil estimar os valores de Km e Vmax nos gráficos não lineares. Isto deu lugar a que vários investigadores concentrassem os seus esforços em desenvolver métodos de linearização da equação de Michaelis-Menten, dando como resultado o gráfico de Lineweaver-Burke, o diagrama de Eadie-Hofstee e o gráfico de Hanes-Woolf. Com o seguinte tutorial da cinética de Michaelis-Menten realizado na Universidade de Virgínia a, pode-se simular o comportamento de uma enzima variando as constantes cinéticas.
O gráfico de Lineweaver-Burk ou representação de duplo recíproco é a forma mais comum, e simples,de mostrar os dados cinéticos, apesar de não ser a mais fiável. Para tal, tomam-se os valores inversos de ambos os lados da equação de Michaelis-Menten. Como se pode apreciar na figura da direita, o resultado deste tipo de representação é uma linha recta cuja equação é e = mx + c, sendo o ponto de intercepção entre a recta e o eixo das ordenadas equivalente a 1/Vmax, e o ponto de intercepção entre a recta e o eixo de abcissas equivalente a -1/Km.
- {\displaystyle {\frac {1}{v}}={\frac {K_{m}}{V_{max}[{\mbox{S}}]}}+{\frac {1}{V_{max}}}}
Evidentemente não se podem tomar valores negativos para 1/[S]; o mínimo valor possível é 1/[S] = 0, que corresponderia a uma concentração infinita de substrato, e daí 1/v = 1/Vmax. O valor do ponto de intercepção entre a recta e o eixo x é uma extrapolação de dados experimentais obtidos em laboratório. Geralmente, os gráficos de Lineweaver-Burke distorcem as medidas realizadas a baixas concentrações de substrato e isto pode dar lugar a estimativas não muito exactas de Vmaxe de Km.[11] Um modelo linear muito mais exacto é o diagrama de Eadie-Hofstee, mas nas investigações científicas actuais, todo este tipo de linearizações tornou-se obsoleto e foi substituído por métodos mais fiáveis baseados na análise de regressão não linear. Para analisar os dados é conveniente a normalização dos mesmos, já que isto pode ajudar à diminuição da quantidade de trabalho experimental a realizar e incremento da fiabilidade da análise,
fonte:
Livro - Princípios de Bioquímica de Lehninger .
RD Resoluções
Foi provado experimental que, para uma concentração específica de enzima, o aumento da concentração de substrato (\(S\)) leva a um aumento na velocidade inicial (\(V_0\)) da reação catalisada pela enzima. Essa função resulta na equação:
\(V_0=V_{max}.\frac{[S]}{[S]+Km}\)
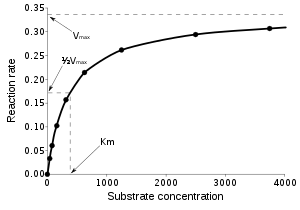
onde km é a constante de Michaelis. O gráfico de Michaelis é:
Figura 1: gráfico de Michaelis

É impossível determinar Vmáx a partir do gráfico da Figura 1. O que podemos fazer nesse caso, é usar o chamado gráfico de Lineweaver-Burk que nada mais é do que uma representação linear da equação de Michaelis-Menten.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta







Compartilhar