como balancear h2c2o4+kmno4+co2
💡 2 Respostas
BRUNO DIAS DO NASCIMENTO
2MnO4- + 5H2C2O4 + 6H+ _ 2Mn2+ + 10CO2 + 8H2O
Especialistas PD
Para começarmos, vamos escrever a equação corretamente:
H2C2O4 + KMnO4 → CO2 + MnO + K2O + H2O
É uma reação de oxirredução, onde ocorre uma oxidação (perda de elétrons) e uma redução (ganho de elétrons) simultaneamente.
Para balancearmos esse tipo de reação, podemos seguir algumas regras:
1º passo) Calcular o Nox de todos os elementos e determinar a variação do Nox (quem se reduz e quem se oxida).
2º passo) Calcular a variação total do Nox (Δ)
Δ = (variação do Nox do elemento) x (nº átomos do elemento na molécula).
3º passo) Tornar o Δ do oxidante como coeficiente do redutor e vice-versa.
Obs: Qual lado da equação usar o coeficiente?
- ao lado do elemento cujo Nox não se repete na equação;
- no elemento com maior atomicidade (maior número de átomos).
4º passo) Prosseguir o balanceamento pelo método das tentativas.
Então temos:
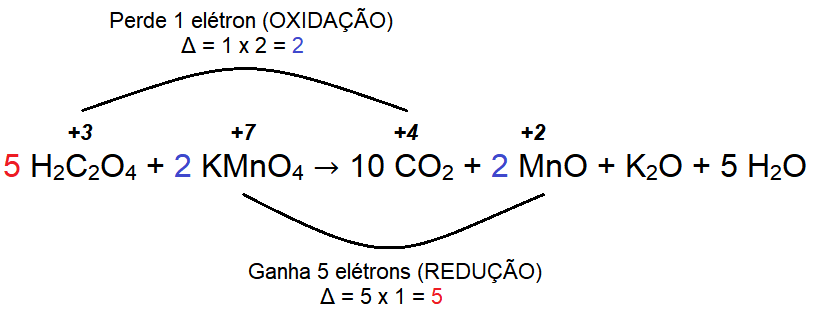
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta





Compartilhar