Determine o pH e o pOH das seguintes soluções:
0,086 g/L de KOH
1,45% (m/v) de HCl
0,5 M de CH3COOH
0,2 M de NaCH3COO
Respostas
Passei Direto
há 8 anos
Nas 2 primeiras situações temos um ácido e uma base fortes (se dissociam completamente em água, então a concentração do ácido/base será igual a concentração de íons H3O+/OH-, respectivamente), então podemos calcular o pH e o pOH de forma direta, sabendo que:
pH = - log [H3O+] pOH = - log [OH-] pH + pOH = 14

Já nas duas últimas situações temos um ácido e uma base fracos, então não podemos proceder com os cálculos da mesma forma. Agora precisamos dos valores de Ka (para ácidos) e Kb (para bases) para determinar a concentração de H3O+ e OH-, através das expressões de Ka e Kb.
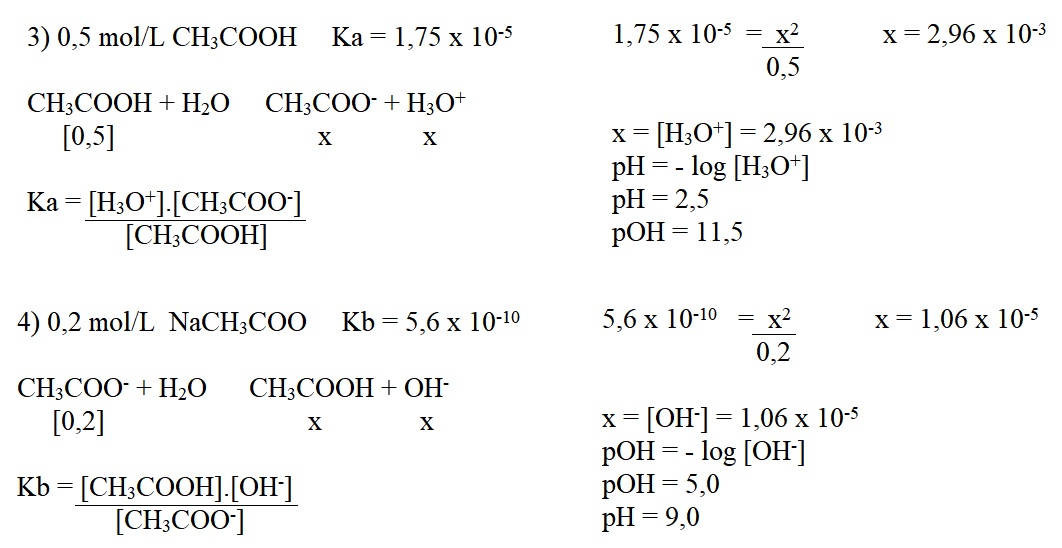

Libere essa resposta sem enrolação!


Cadastre-se ou realize login
Ao continuar, você aceita os Termos de Uso e Política de Privacidade






