Respostas
Especialistas PD
Em um cálculo estequiométrico, primeiro temos que montar a equação química que corresponte a este processo e balancea-la. Após estabelecemos as relações e obtemos os valores desejados.
Atenção! Óxido de ferro III - Fe2O3 (não é dióxido, como dito no enunciado, e sim um trióxido).
Através da reação balanceada entre o óxido de ferro III e o carbono, gerando ferro e dióxido de carbono, percebemos que a cada 2 mols de óxido de ferro III que reagem, são produzidos 4 mols de Fe! Calculando suas massas molares (valores tabelados), podemos fazer a relação de que 2 x 160g de Fe2O3 formam 4 x 56 g de Fe. Então quanto de Fe2O3 seria necessário para formar 10g de Fe? Resolvendo a regra de três, obtemos o valor de aproximadamente 14,3 g.
E de modo semelhante obtemos a massa de CO2 formada quando reagimos 14,3 g de óxido de ferro III, que é igual a 5,9 g.
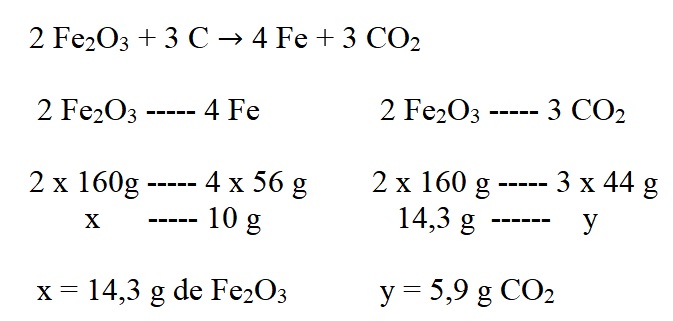
Responda
Para escrever sua resposta aqui, entre ou crie uma conta





