calculo o raio de um átomo de irídio dado que ir possui uma estrutura cristalina CFC, uma densidade de 22,4 g/cm^3 e um peso atômico de 192,2 g/mol
💡 3 Respostas
Julio C. Lourenço
Para este exercício temos os seguintes dados:
Material: irídio
Estrutura cristalina: CFC (4 átomos por célula unitária)
Densidade (massa específica, ρ): 22,4 g/cm³
Peso atômico (A): 192,2 g/mol
Para este exercício aplicaremos inicialmente a fórmula de massa específica (retirado do livro do Callister):
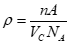
Utilizando os valores e resolvendo para Vc (Volume da célula unitária), teremos:
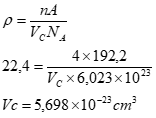
Sabendo que o volume da célula unitária corresponde ao parâmetro de rede elevado ao cubo, temos:
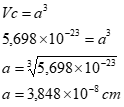
Por fim, para a estrutura CFC, a seguinte relação entre o raio e o parâmetro de rede é válida:
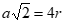
Substituindo, encontraremos que 4 corresponde a:
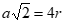
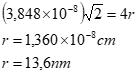
Alvaro Barbosa de Castro Filho
Sabemos que estrutura de "CFC" possui sua aresta
Pela formula de densidade temos que:
Onde:
"N" = total de atomos em cada célula unitaria
"A" = peso atomico
Na = numero de avogadro
Vc = volume total da célula unitaria
Em um "CFC" temos 8 atomos nos vertices e 6 atomos em cada face:
Na ≈ 6,0*10²³
Levando os dados na formula da densidade ficamos:
64R³/2√2 = 0,05720cm³/10²¹
32R³/√2 = 0,05720cm³/10²¹
32R³ = √2*0,05720cm³/10²¹
R³ = √2*0,05720cm³/(10²¹*32)
R³ ≈ 0,08089cm³/(10²¹*32)
R³ ≈ 0,0025cm³/(10²¹)
R³ ≈ 2,5*10⁻³cm³/(10²¹)
R³ ≈ 2,5cm³/(10³*10²¹)
R³ ≈ 2,5cm³/(10²⁴)
R ≈ ∛2,5cm³/∛(10²⁴)
R ≈ ∛2,5*cm/10⁸
R ≈ 1,35720cm/10⁸
R ≈ 1,35*10⁻⁸cm
Bárbara Lenoir
Para calcular o raio de um átomo de irídio (Ir) com base na estrutura cristalina CFC (cúbica de faces centradas), podemos usar a fórmula da densidade e relacioná-la com a fórmula da célula unitária CFC.
Em uma estrutura CFC, existem átomos nos vértices de um cubo e também nos centros das faces desse cubo. Cada átomo de canto é compartilhado por oito células unitárias, enquanto cada átomo de face é compartilhado por duas células unitárias. Portanto, o número total de átomos na célula unitária CFC é:
Número de átomos na célula unitária CFC = (8 x número de átomos nos vértices) + (2 x número de átomos nas faces)
No caso do irídio (Ir), cada átomo nos vértices é compartilhado com oito células unitárias e cada átomo nas faces é compartilhado com duas células unitárias. Portanto, o número total de átomos na célula unitária CFC de irídio é:
Número de átomos na célula unitária CFC de Ir = (8 x 1) + (2 x 1) = 10 átomos
A massa de uma célula unitária CFC é igual ao peso atômico em gramas multiplicado pelo número de átomos na célula unitária CFC. Portanto, a massa de uma célula unitária CFC de irídio é:
Massa da célula unitária CFC de Ir = peso atômico do Ir x número de átomos na célula unitária CFC de Ir
Massa da célula unitária CFC de Ir = 192,2 g/mol x 10 átomos = 1922 g
A densidade de um material é definida como a massa dividida pelo volume. Podemos rearranjar essa fórmula para encontrar o volume da célula unitária CFC:
Volume da célula unitária CFC = massa da célula unitária CFC de Ir / densidade de Ir
Volume da célula unitária CFC = 1922 g / 22,4 g/cm³ = 85,8929 cm³
Em uma célula unitária CFC, o átomo está localizado no centro de cada face do cubo, o que corresponde a um quarto de um átomo em termos de volume. Portanto, o volume ocupado por um único átomo de irídio é:
Volume ocupado por um átomo de Ir = Volume da célula unitária CFC / número de átomos na célula unitária CFC de Ir
Volume ocupado por um átomo de Ir = 85,8929 cm³ / 10 átomos = 8,58929 cm³
O raio de um átomo de irídio pode ser calculado usando a fórmula do volume de uma esfera:
Volume de uma esfera = (4/3) x π x raio³
Podemos rearranjar essa fórmula para encontrar o raio:
Raio = (3 x Volume ocupado por um átomo de Ir / (4 x π))^(1/3)
Raio = (3 x 8,58929 cm³ / (4 x 3,14159))^(1/3)
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Calcule o raio de um átomo de irídio dado que o Ir possui uma estrutura cristalina CFC, uma densidade de 2,4g/cm3, em um peso atômico de 192,2g/mol
Fundamentos de Ciências dos Materiais
•UNIFACVEST
kellen Figueredo





Compartilhar