Discuta a ligação e a geometria na molécula de pentacloreto de fósforo, ???5.
💡 2 Respostas
Especialistas PD
Estrutura de Lewis PCl5:
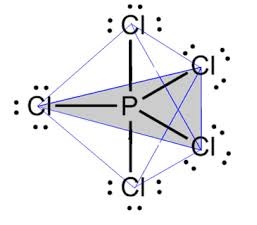
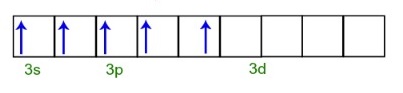
O fósforo (P) possui 5 elétrons na sua camada de valência, e o cloro (Cl), 7 elétrons. Nesta molécula cada átomo de cloro possui 3 pares de elétrons não ligantes. Aplicando a teoria VSEPR, temos ligações entre o fósforo e o cloro num ângulo de 90º e outras de 120º, formando uma bipirâmide de base triangular, geometria bipirâmide trigonal. Nessa molécula o fósforo sofreu hibridização, pois realizou cinco ligações. Ao receberem energia do meio externo, os elétrons do átomo de fósforo excitam-se. Logo em seguida, um dos dois elétrons pertencentes ao subnível 3s desloca-se para um orbital vazio presente no subnível d, que até então não possui nenhum elétron. Nesse momento, temos na camada de valência do fósforo um orbital s, três orbitais p e um orbital d incompleto. Por fim, esses cinco orbitais hibridizam-se, ou seja, unem-se, resultando então em cinco orbitais atômicos incompletos, que são capazes agora de realizar cinco ligações químicas. Como foram unidos um orbital s, três orbitais p e um orbital d, a hibridização do Fósforo é do tipo sp3d.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 4 pág.
4 pág.






Compartilhar