Resolvendo a equação química da reação do sulfato de prata com Cobre, gerando sulfato de cobre mais prata, representada abaixo: qual a alternativa?
💡 4 Respostas
Djalma Oliveira
Letra C está correta com uma correção pequena. Vejamos abaixo:
Eletrodo de redução: 2Ag+ +2e- --> 2 Ago
Eletrodo de oxidação: Cuo --> Cu2+ + 2e-
A soma é a reação da célula completa ou pilha: 2Ag+ + Cu --> 2Ago + Cu2+
Camila Assis
Alternativa: c
O método íon-elétron baseia-se na divisão da reação global de oxirredução em duas semi-equações.
O primeiro passo é identificar as espécies que sofrem oxidação e redução:
Ag2SO4 + Cu → CuSO4 + Ag
A prata, passa de +1 para zero, recebe elétron, redução. Já o cobre passa de zero para +2, perde elétron, oxidação.
Vamos escrever as semi-reações de redução e de oxidação:
2 Ag+ + 2e- → 2 Ag0 (cada Ag recebe 1 elétron, temos 2 Ag nos reagentes, por isso balanceamos a semi-reação!)
Cu0 → Cu2+ + 2e-
Somando as duas semi-reações, cancelando os elétrons cedidos e recebidos, temos a reação final.
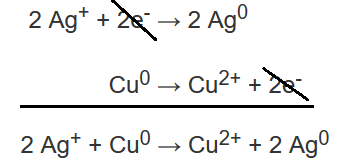
lenilson moreira
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 2 pág.
2 pág.





Compartilhar