Nomeie as substâncias?
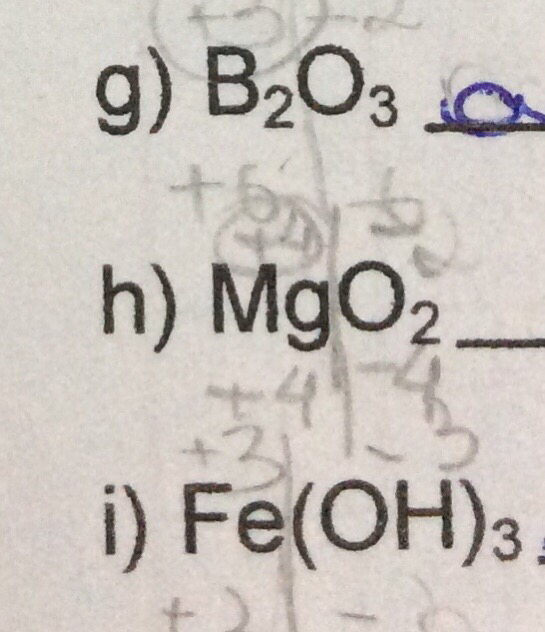
💡 5 Respostas
Judalino Pacheco
Óxido de Boro, Óxido de Magnésio, e Hidróxido de Ferro
Andre Smaira
------
A forma padrão de nomeação de um óxido segue a regra: prefixo que indica a quantidade de oxigênios + “óxido de” + prefixo que indica quantidade do outro elemento + nome do outro elemento. Em casos que o número do elemento ligado ao oxigênio pode ser deduzido a partir da análise das valências, dispensa-se o prefixo ao nome do elemento
------
No caso de bases, o nomeação se dará por: “hidróxido de” + nome do elemento ligado
------
Nos casos de óxidos ou bases em que o oxigênio ou íon, respectivamente, possuam mais de uma valência, indicamos, ao final, tal número em algarismos romanos. Caso ele seja a maior valência possível, podemos substituir o número pelo pós-fixo “ico” ao final do nome do elemento. Caso seja a menor, utilizamos “oso”.
------
Sabendo disso, analisemos os itens:
------
a) \(B_2O_3\): pela regra, teríamos Trióxido de diboro. Podemos simplifica-lo para Trióxido de boro.
------
b) \(MgO_2\): pela regra, teríamos Dióxido de magnésio. Esse composto, porém, é classificado como um peróxido (composto binário de oxigênio com metal alcalino) e seu nome será Peróxido de magnésio.
------
c) \(Fe(OH)_3\): pela regra, temos Hidróxido de Ferro (III). Como 3 é a maior valência possível do Ferro em óxidos, também podemos chama-lo de Hidróxido férrico.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 9 pág.
9 pág. 5 pág.
5 pág.
Compartilhar