Calcule as concentrações de Cd2+, [Cd(CN)42-] e CN- no equilíbrio
💡 5 Respostas
Felipe Gonçalves Ferreira
[Cd²⁺] = 0,42 mol / 1 L = 0,42 M
Cd²⁺(aq) + 4 CN⁻(aq) -----------> Cd(CN)₄²⁻(aq)
↓ ↓ ↓
inicio : 0,42 M 2,50 M 0
v : -0,42 M -4 (0,42)M + 0,42
____________________________________________
final 0 0,82 M 0,42 M
Para encontrar a concentração destas espécies em equilíbrio, re-equilibramos [Cd²⁺] obs:não pode usar o zero na constante de formação:
Cd²⁺(aq) + 4 CN⁻(aq) ⇄ Cd(CN)₄²⁻(aq)
↓ ↓ ↓
inicio 0 0,82 M 0,42 M
V + x + 4 x - x
__________________________________________
Eq : x 0,82 + 4 x 0,42 - x
Utilizando a constante de complexação ( Kf ) :
[ Cd²⁺ ] = 0,42 / ( 7,1 x 10¹⁶) ( 0,82)⁴
[ Cd²⁺ ] = 1,30 x 10⁻¹⁷ M
[ CN⁻ ] = 0,82 + 4 ( 1,30 x 10⁻¹⁷ )
[ CN⁻ ] = 0,82 M
[ Cd(CN)₄⁻²] = 0,42 - ( 1,30 x 10⁻¹⁷ )
[ Cd(CN)₄⁻²] = 0,42 M
Andre Smaira
Além disso, temos a equação química \(C{d^{2 + }}(aq) + 4C{N^ - }(aq) \to Cd(CN)_4^{2 - }(aq)\).
Com isso, temos que:
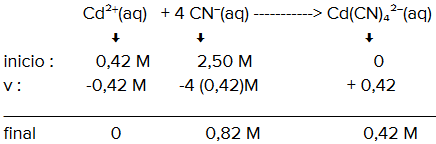
cálculo das concentrações
Então, para encontrar o equilíbrio destes compostos, nesta etapa, teremos:
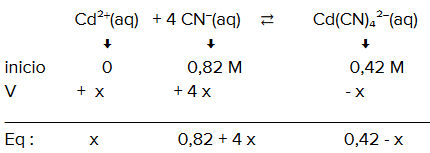
segundo cálculo das concentrações
Com isso, a partir da constante de complexação, temos:
\[\left[ {C{d^{2 + }}} \right] = \dfrac{{0,42}}{{\left( {7,1 \cdot {{10}^{16}}} \right) \cdot ({{0,82}^4})}} = \boxed{1,30 \cdot {{10}^{ - 17}}M}\]
\[\left[ {C{N^ - }} \right] = 0,82 + 4 \cdot (1,3 \cdot {10^{ - 17}}) = \boxed{0,82M}\]
\[\left[ {Cd\left( {CN} \right)_4^{ - 2}} \right] = 0,42 - 4 \cdot (1,3 \cdot {10^{ - 17}}) = \boxed{0,42M}\]
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Calcule as concentrações de [H+] e [OH-] em uma solução de pH=5,6.
Química Analítica I
•UEM
João Vitor Silva




Compartilhar