Duvida em atividade de QUIMICA 2° ano do EM
02) Uma mistura constituída de 45 g de cloreto de sódio e 100 mL de água, contida em um balão e inicialmente a 20 °C, foi submetida à destilação simples, sob pressão de 700 mm Hg, até que fossem recolhidos 50 mL de destilado (líquido). O esquema a seguir representa o conteúdo do balão de destilação, antes do aquecimento:
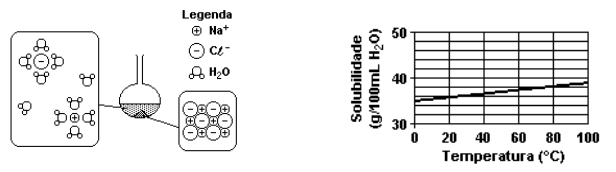
Qual a massa de cloreto de sódio cristalizada, a 20 °C, após terem sido recolhidos 50 mL de destilado (líquido)? Justifique.
💡 5 Respostas
Rafael Izidoro
Solubilidade (20º) do NaCl, pelo gráfico: 36 g / 100 mL (H2O).
A destilação permitiu a obtenção de 50 mL de água, logo, restam 50 mL de água na mistura.
M(NaCl dissolvida) / 50 mL = 36 g / 100 mL
M(NaCl dissolvida) = 18 g de NaCl(aq) (após obtenção de 50 mL de H2O destilada).
No início, têm-se 45 g de NaCl em 100 mL de H2O, logo, Mnão dissolvida = 45g - 36g = 9 g
Porém, a cristalização ocorre somente a partir dos íons aquosos, ou seja, Na+(aq) + Cl-(aq) → NaCl(s)
Os 9 g JÁ ESTAVAM cristalizados, antes da destilação proceder. O enunciado exige a massa que CRISTALIZOU após o procedimento.
Logo, para saber quanto cristaliza, devemos analisar a massa dos íons dissolvidos no início e no fim:
M(cristalizada) = M(inicial) - M(final)
M(cristalizada) = 36 g - 18 g = 18 g
18 g solidificaram-se.
Andre Smaira
Sabendo disso, basta fazer uma regra de três. Sabendo que \(36\text{ g}\) de cloreto de sódio estão para \(100\text{ mL}\) de solução, impõe-se que \(x\) gramas está para \(50\text{ mL}\) de solução. Fazendo isso, vem que:
\[\eqalign{ & x = \dfrac{{50 \cdot 36}}{{100}} \cr & = 18{\text{ g}} }\]
Por fim, basta subtrair o que foi solubilizado da massa total da mistura para determinar a massa de cloreto de sódio cristalizado:
\[45{\text{g}} - 18{\text{g}} = 27{\text{g}}\]
Portanto, \(\boxed{27\text{ g}}\) de cloreto de sódio foram solubilizadas.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar