Explique por que a molécula de água se comporta de forma diferente com os íons Na+ e Cl-
💡 4 Respostas
Mateus Barbosa
Se você misturar sal em água, a estrutura cristalina do NaCl vai começar a se dissociar em íons Na^++start superscript, plus, end superscript e Cl^-−start superscript, minus, end superscript. (Dissociação é apenas um nome para o processo no qual um composto ou molécula se separa para formar íons.) As moléculas de água formam camadas de solvatação em torno dos íons: íons Na^++start superscript, plus, end superscriptpositivamente carregados são rodeados pelas cargas parcialmente negativas da extremidades oxigênio das moléculas de água, enquanto os íons Cl^-−start superscript, minus, end superscriptnegativamente carregados são rodeados pelas cargas parcialmente positivas das extremidades hidrogênio. À medida que o processo continua, todos os íons dos cristais do sal de cozinha são envolvidos por camadas de solvatação e dispersados na solução.
Moléculas apolares, como gorduras e óleos, não interagem com a água e não formam camadas de solvatação. Essas moléculas não possuem regiões com cargas parciais positivas ou negativas, então elas não são atraídas eletrostaticamente pelas moléculas de água. Assim, em vez de dissolver-se, substâncias apolares (como, por ex., os óleos) permanecem separadas e formam camadas ou gotículas quando acrescentadas à água.
Andre Smaira
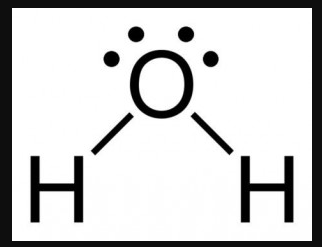
Água
Nota-se que a molécula fica polarizada e se divide em uma região positiva(vermelho) onde estão os átomos de hidrogênio e outra região negativa(azul) onde estão os elétrons do átomo de oxigênio:
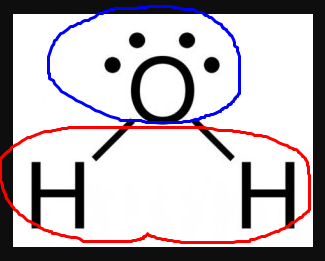
polarizaçao
Cada região vai interagir de forma diferente com íons $Cl^-$ e $Na^+$, considerando que regiões com polarizações opostas se atraem e regiões com polarizações iguais se repelem. A região positiva será atraída para os íons de cloro, já a região negativa será atraída para os íons de sódio.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 1 pág.
1 pág. 1 pág.
1 pág.




Compartilhar