(UERJ 2013) O cobre metálico é obtido a partir do sulfeto de cobre I em duas etapas subsequentes, representadas pelas seguintes equações químicas:
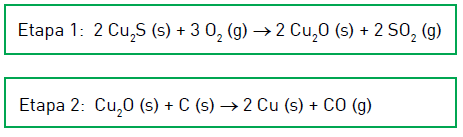
Em uma unidade industrial, 477 kg de Cu\(_2\)S reagiram com 100% de rendimento em cada uma das etapas.
Nomeie os dois gases formados nesse processo. Em seguida, calcule o volume, em litros, de cada um desses gases, admitindo comportamento ideal e condições normais de temperatura e pressão.
Respostas
Estudante PD
há 6 anos
Multiplicando por dois a equação da segunda etapa, anulamos o composto intermediário e, determinamos a equação global do processo:

Consultando a tabela periódica, calculamos a massa molar do Cu2S e, considerando CNTP, proporcionamos:
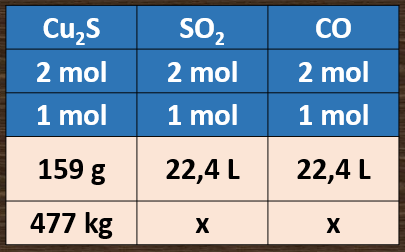

Nomenclatura dos gases:
SO2 = Dióxido de enxofre
CO = Monóxido de carbono


Crie sua conta grátis para liberar essa resposta. 🤩
Já tem uma conta?
Ao continuar, você aceita os Termos de Uso e Política de Privacidade
Leonardo DT
há 6 anos
Isso é distribuição de carbono ??
Juliana Cortez
há 6 anos
Acho q é sim





