Respostas
Guilherme Cordeiro
Vi que a questão é de faculdade e mesmo estando no ensino médio, vou arriscar a responder:
primeiramente vamos usar a formula de clapeyron:
pV= nRT
no caso calculando nas condições iniciais, 1 mol, 300k, e 22,0L
ficaria de jeito na formula:
P1 x 22 = 1x 0,082 x 300
p1= 1,119 atm
no caso calculando nas condições finais, 1 mol, 300k e 30L
ficaria desse jeito na formula:
P2 x 30 = 1x 0,082 x 300
p2 = 0,82 atm
olhando num gráfico fica da seguinte forma os dados de pressão e volume para o calculo de trabalho:
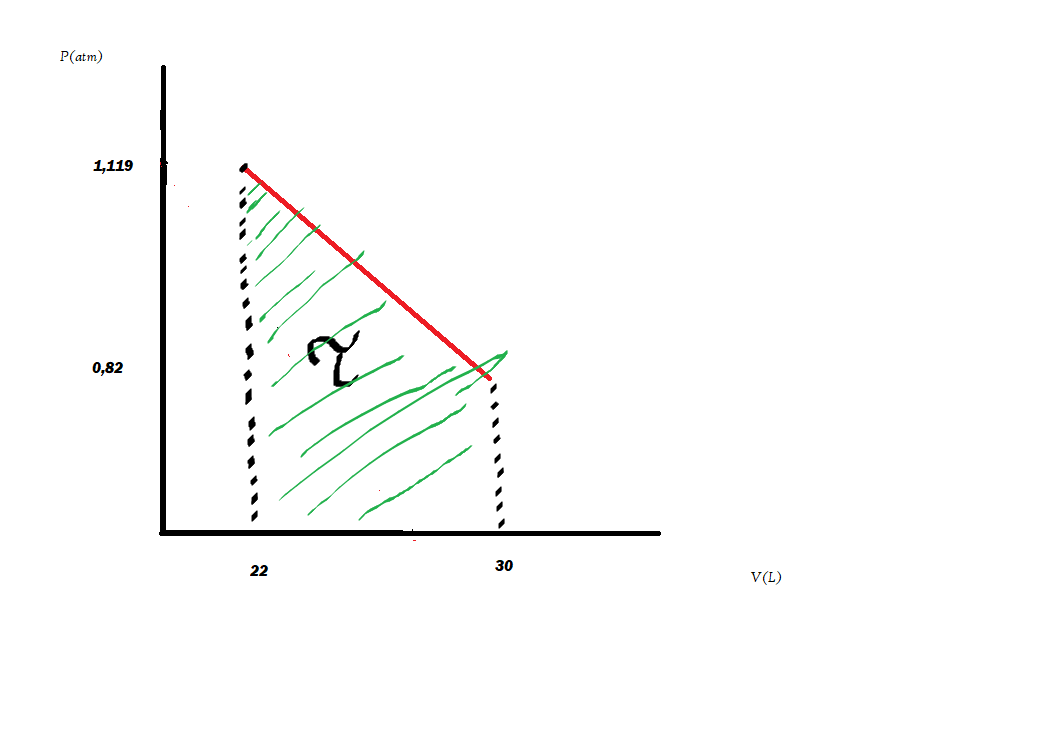
perdoe a primitivez do gráfico kkkkk
agora bastra calcular a área do trapézio, que dá 7,756 Joules
agora o calor cai na regra de transformções isotermicas, ou seja, todo calor recebido é convertido integralmente entrabalho ou do trabalho exercido pelo meio sobre o sistema é liberado na forma de calor. Logo, o calo também é 7, 756 joules
Andre Smaira
\[\boxed{\tau=Q}\]
Considerando a fórmula a seguir e que a constante dos gases perfeitos, seja, \(R=0,082\ \dfrac{atm.L}{mol.K}\) é possível encontrar o valor inicial e final da pressão do gás.
\[P.V=n.R.T\]
\[P_i=\dfrac{1\ .\ 0,082\ .\ 300}{22}\]
\[\boxed{P_i=\dfrac{24,6}{22}\ atm}\]
A pressão final seria, então:
\[P_f=\dfrac{1\ .\ 0,082\ .\ 300}{30}\]
\[\boxed{P_f=\dfrac{24,6}{30}\ atm}\]
Com as duas pressões é possível encontrar o valor do trabalho realizado nessa expansão isotérmica com a seguinte fórmula e considerando \(R=8,31\ \dfrac{J}{mol.K}\):
\[\boxed{W=n.R.T.ln(\dfrac{P_i}{P_f})}\]
\[W=1\ .\ 8,31\ .\ 300\ .\ ln(\dfrac{\dfrac{24,6}{22}}{\dfrac{24,6}{30}})\]
\[\boxed{W=773,2162\ J}\]
Como o gás está expandindo o valor do trabalho é positivo e o calor fornecido para esse gás é numericamente igual ao trabalho:
Responda
Para escrever sua resposta aqui, entre ou crie uma conta






