Nos gases produzidos por fábricas e motores
(em especial quando há queima de carvão mineral) são liberados para a atmosfera óxidos de enxofre (SO 2 ) os quais reagem com o vapor da água produzindo ácido sulfúrico (H 2 SO 4 ), que é diluído na água da chuva e dando origem a chuva ácida, com pH muito ácido. As equações químicas de formação da chuva ácida são representadas por:
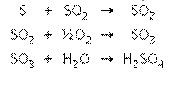
Na formação de 98 g de H 2 SO 4 , são reagidos quantas gramas de oxigênio?
|
( ) a) 64 g. |
||
|
( ) b) 98 g. |
||
|
( ) c) 16 g. |
||
|
( ) d) 32 g. |
||
|
( ) e) 49 g. |
💡 3 Respostas
Andre Smaira
Dados:
- massa atômica dos elementos:
- H: 1 u
- S: 32 u
- O: 16 u
- massa molar:
- H2SO4:
\(2\times 2+32+4\times 16=98 {\ g/mol}\) - O2:
\(2 \times 16=32 {\ g/mol}\)
O número de mols
\(n\)
presente em 98 g de H2SO4 é :
\[n=\dfrac{98 {\ g}}{98 {\ g/mol}}=1 {\ mol}\]
A reação de formação do H2SO4 é:
\[{{S}}{{{O}}_3} + {{{H}}_2}{{O}} \to {{{H}}_2}{{S}}{{{O}}_4}\]
Por esta reação, sabe-se que para cada mol de H2SO4 requer um mol de SO3 como reagente.
Por outro lado, a reação que forma SO3 é:
\[{{S}}{{{O}}_2} + {{^1/_2{O}}_2} \to {{S}}{{{O}}_3}\]
Assim, um mol de SO3 requer 0,5 mol de oxigênio (O2).
Assim, sabe-se que na formação de 98 g de H2SO4 são reagidos 0,5 mol de oxigênio. Como a massa molar do oxigênio é 32 g/mol, a massa de oxigênio que deve reagir é:
\[m= 0,5 {\ mol} \times 32 {\ g/mol}=16 {\ g}\]
Portanto, a alternativa certa é C) 16 g.
Japa Caudilio Caudilio
Randália Pereira
c) 16 g
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas dessa disciplina
Conteúdos escolhidos para você
 3 pág.
3 pág. 5 pág.
5 pág. 55 pág.
55 pág.



Compartilhar