O hidreto de cálcio é um composto comumente usado para encher balões, pois sua reação com água fornece muito hidrogênio em relação ao seu peso.
A equação química pode ser representada por na equação:
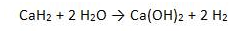
Assinale a alternativa que apresenta a quantidade produzida de hidrogênio, ao reagir-se 84 g de CaH 2 e 96 g de H 2 O:
|
( ) a) 16 g. |
||
|
( ) b) 11 g. |
||
|
( ) c) 8 g. |
||
|
( ) d) 72 g. |
||
|
( ) e) 4 g. |
💡 15 Respostas
Fernanda Câmara Cardozo
Andre Smaira
Dados:
- massas atômicas:
- Ca: 40u;
- H: 1u;
- O: 16u;
- massas molares:
- CaH2:
\(40 +2\times 1=42 {\ g/mol}\)
; - H2O:
\(2 \times 1+16=18 {\ g/mol}\)
; - H2:
\(2 \times 1=2 {\ g/mol}\)
.
O número de mols de hidreto de água disponíveis é:
\[n_{{CaH}_2}=\dfrac{84 {\ g}}{42 {\ g/mol}}=2 {\ mols}\]
O número de mols de água é:
\[n_{{H}_2 {O}}=\dfrac{96 {\ g}}{18 {\ g/mol}}=5,33 {\ mols}\]
Como
\(\dfrac{n_{{H}_2 {O}}}{n_{{CaH}_2}}=2,67\)
, observa-se que as quantidades de água e hidreto de cálcio disponíveis não seguem a proporção estequiométrica de 2:1. Portanto, temos água em excesso e o hidreto de cálcio é o reagente limitante da reação.
A equação da reação mostra que para cada mol de CaH2 forma-se dois mols de H2. Portanto, com 2 mols de CaH2 serão formados
\(2 \times 2=4\)
mols de H2.
A massa de H2 formada será. portanto:
\[m= 4 {\ mols }\times 2 {\ g/mol}=8 {\ g}\]
Portanto, a alternativa correta é C) 8g.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
O hidreto de cálcio é um composto comumente usado para encher balões, pois sua reação com água fornece muito hidrogênio em relação ao seu peso. A e...
Fundamentação Química Aplicada à Prática Biomédica
Progresso com Exercícios
Materiais relacionados
 1 pág.
1 pág. 1 pág.
1 pág. 1 pág.
1 pág.




Compartilhar