Certo gás monoatômico e ideal sofre uma transformação termodinâmica na qual seu volume permanece constante. ?
Certo gás monoatômico e ideal sofre uma transformação termodinâmica na qual seu volume permanece constante. Durante o processo, o gás cede 20 calorias para o meio externo. Qual a variação da energia interna, a quantidade de calor envolvido no processo e o trabalho realizado sobre ou pelo gás, respectivamente.
Sua resposta
💡 3 Respostas
RICARDO APARECIDO PEREIRA
É preciso saber quanto de calor ele absorveu ou como mudou a temperatura. Essas duas variáveis dependem uma da outra e não tem como saber uma sem a outra. O trabalho realizado/sofrido pelo gás é zero pois não houve variação do volume.
Alice Almeida de Lima
Enquanto o número de graus de liberdade de um gás (quantidade de direções que as moléculas de um gás podem transladar, rotacionar e vibrar) afeta a fórmula utilizada para o cálculo de sua energia interna, a quantidade de calor recebida por ele durante uma transformação isovolumétrica é exatamente igual à quantidade de calor recebida ou cedida por ele. Dizemos que, quando um gás recebe calor, sua energia interna sofre um acréscimo, portanto, apresentará sinal positivo. A Primeira Lei da Termodinâmica para gases ideais que sofrem transformações isovolumétricas é dada por:
Legenda:
ΔU – variação da energia interna do gás (J – joules)
Q – calor recebido ou cedido (J)
Dessa forma, a variação da energia interna do gás é dada pela própria quantidade de calor por ele absorvida: +12,0 J.
Isabela Pereira
-20 -20 0
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
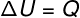





Compartilhar