Os produtos de uma reação entre íons brometo e íons permanganato em solução aquosa básica são óxido de manganês (IV) sólido e íons bromato.
Os produtos de uma reação entre íons brometo e íons permanganato em solução aquosa básica são óxido de manganês (IV) sólido e íons bromato. Balanceie a equação.
💡 2 Respostas
bruna
...
Especialistas PD
Inicialmente, verifica-se quem se oxida e quem se reduz. A seguir escreve-se a semi-reação de oxidação e a de redução.
Br- + MnO4- → MnO2 + BrO3-
Semi-reação de oxidação:
Etapa 1 - Identificar as espécies que se oxidam: o número de oxidação do bromo vai de -1 para +5, perde elétrons = oxidação.
Etapa 2 - Escrever a equação simplificada da oxidação: Br- → BrO3-
Etapa 3 - Balancear todos os elementos, exceto H e O. Verifica-se que o bromo já está balanceado. Então, vamos para a etapa 4.
Etapa 4 - Balancear oxigênio, para cada átomo, adiciona-se duas hidroxilas ao lado deficiente em oxigênio, e uma molécula de H2O ao lado oposto.
Br- + 6 OH- → BrO3- + 3 H2O
Agora, balancear H. Para cada átomo, adiciona-se uma molécula de água ao lado deficiente em hidrogênio e uma hidroxila ao lado oposto. Nessa reação o hidrogênio já está balanceado!
Etapa 5 - Balancear as cargas adicionando elétrons no lado deficiente.
Br- + 6 OH- → BrO3- + 3 H2O + 6e-
Semi-reação de redução:
Etapa 1 - Identificar as espécies que se reduzem: o número de oxidação do manganês vai de +7 para +4, ganha elétrons = redução.
Etapa 2 - Escrever a equação simplificada da oxidação: MnO4- → MnO2
Etapa 3 - Balancear todos os elementos, exceto H e O. Verifica-se que o manganês já está balanceado. Então, vamos para a etapa 4.
Etapa 4 - Balancear oxigênio, para cada átomo, adiciona-se duas hidroxilas ao lado deficiente em oxigênio, e uma molécula de H2O ao lado oposto.
MnO4- + 2 H2O → MnO2 + 4 OH-
Agora, balancear H. Para cada átomo, adiciona-se uma molécula de água ao lado deficiente em hidrogênio e uma hidroxila ao lado oposto. Nessa reação o hidrogênio já está balanceado!
Etapa 5 - Balancear as cargas adicionando elétrons no lado deficiente.
3e- + MnO4- + 2 H2O → MnO2 + 4 OH-
Etapa 6 - Escrever a equação total. Para isso, verifica-se que nas semi-reações, 2 elétrons são perdidos na oxidação, mas 2 também são ganhos na redução. Basta então somar as duas semi-reações e cancelar os elétrons e íons comuns:
Br- + 6 OH- → BrO3- + 3 H2O + 6e-
3e- + MnO4- + 2 H2O → MnO2 + 4 OH- (x2)
Então temos:
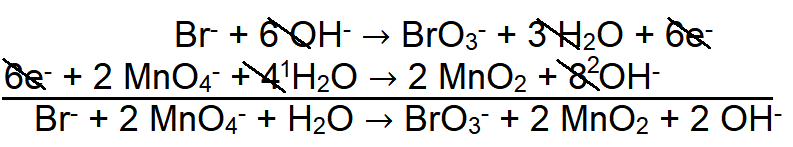
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
utilizar uma solução 0,002 mol/L de permanganato de potássio, será possível determinar a concentração de íons ferro na amostra?
Química Analítica Quantitativa Experimental
Adamilton Alves








Compartilhar