Respostas
Marcio Marçal Lobo
O carbono e o oxigenio são hibridizados sp2 e isso explica a planaridade da molécula do formaldeído. Ocorre a superposição dos orbitais 1s1 dos hidrogênios com os lobos dos orbitais sp2 do carbono... e a superposição dos orbitais sp2 - sp2 carbono-oxigênio
Especialistas PD
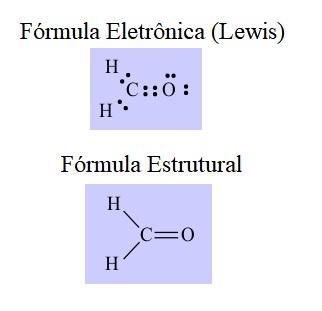
A hibridização do carbono do formaldeído é do tipo sp2, que ocorre quando o carbono tem uma ligação dupla e duas ligações simples ou uma ligação pi (π) e três ligações sigma (σ).
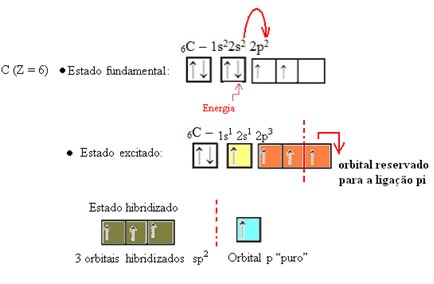
Os átomos de hidrogênio que realizam a ligação simples com o carbono, realizam-na com o seu orbital s. O orbital p “puro” que restou realiza a ligação dupla com o átomo de oxigênio e a molécula de formol fica com a seguinte estrutura:
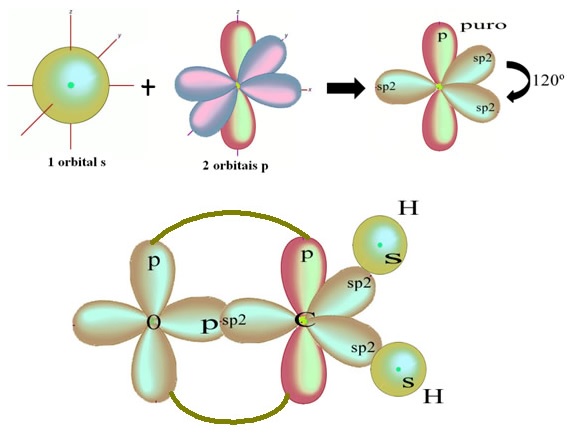
Quanto ao tipo de ligações existentes nessa estrutura do formol, temos: as ligações entre o H e o C são σs-sp2 e as ligações (dupla) entre o C e o O são: σp-sp2 e πp-p
Responda
Para escrever sua resposta aqui, entre ou crie uma conta






