As substâncias utilizadas nos processos químicos de desinfecção da água, nomeie-as (?)
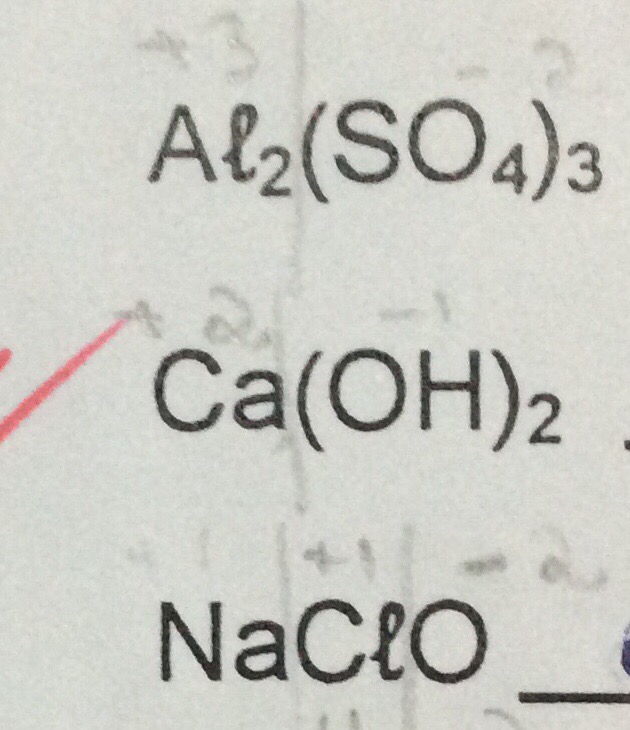
💡 5 Respostas
Judalino Pacheco
Sulfato de Alumínio, Óxido de Cálcio e Cloreto de Sódio
Andre Smaira
------
A forma padrão de nomeação de um óxido segue a regra: prefixo que indica a quantidade de oxigênios + “óxido de” + prefixo que indica quantidade do outro elemento + nome do outro elemento. Em casos que o número do elemento ligado ao oxigênio pode ser deduzido a partir da análise das valências, dispensa-se o prefixo ao nome do elemento.
------
No caso de bases, a nomeação se dará por: “hidróxido de” + nome do elemento ligado.
------
Nos casos de óxidos ou bases em que o oxigênio ou íon, respectivamente, possuam mais de uma valência, indicamos, ao final, tal número em algarismos romanos. Caso ele seja a maior valência possível, podemos substituir o número pelo pós-fixo “ico” ao final do nome do elemento. Caso seja a menor, utilizamos “oso”.
---
No caso de sais, o nome será uma combinação do cátion e ânion que o formam.
----
Sabendo disso, analisemos os itens:
------
a) \(Al_{2}(SO_{4})_{3}\): o composto é um sal formado pelo cátion alumínio Al+3 e pelo ânion sulfato SO4-2. Seu nome será, então, Sulfato de alumínio
------
b) \(Ca(OH)_{2}\): pela regra, temos Hidróxido de cálcio.
------
c) \(NaClO\): o composto é um sal formado pelo cátion sódio Na+ e pelo ânion hipoclorito ClO-. Pela regra, temos que seu nome será Hipoclorito de Sódio.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 11 pág.
11 pág.






Compartilhar