Dado o conjunto de número quânticos do elétron mais energético de um átomo qualquer: n = 3; l = 1 ; ml = 0 ; ms = + ½
qual a sua configuração eletrônica?
💡 1 Resposta
Camila Assis
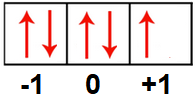
Pelo conjunto de números quânticos, temos que o número quântico principal é igual a 3, então o elétron mais energético, está no terceiro nível, ou terceira camada. Como o número quântico secundário, l, é 1, temos o subnível d. Até então 3d. O número quântico magnético é 0, ou seja, o último elétron está no orbital zero e o spin é + ½, o elétron está pra baixo, segundo o diagrama de caixas, onde este elétron é o quinto a ser distribuído: 3d5.
Fazendo a distribuição eletrônica até o subnível 3d5 (mais energético) teremos: 1s2 2s2 2p6 3s2 3p5, com um total de 17 elétrons. Então este átomo, também com 17 prótons e número atômico 17, é o cloro. Quer saber mais?
Entre no link https://www.passeidireto.com/video/45459387/numeros-quanticos-teoria
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta






Compartilhar