Com a estrutura molecular do indicador de vermelho de fenol, descreva a reação de protonação e desprotonação, indicando a coloração de cada forma
💡 2 Respostas
Leticia Sanches
O vermelho de fenol pode ser usado como indicador da presença de células produtas de ácidos, mudando de cor para amarelo devido a presença dos compostos ácidos produzidos por tais células.
Em química, uma protonação é uma reação química que ocorre quando um próton (H+) liga-se a um átomo, uma molécula ou um íon. O produto desta reação é chamado ácido conjugado do reagente inicial. É possivelmente a reação química mais fundamental e é um passo em muitos processos estequiométricos e catalíticos.
Protonando-se a ligação de B pelo ácido AH, resultando um protonado.
A reação inversa é a desprotonação, quando um próton, novamente H+, é removido de uma molécula ou de um íon.
Ácido clorídrico entrega um próton para a molécula de amônia. Então resulta um íon cloro negativamente carregado assim como um cátion amônio positivamente carregado.
Andre Smaira
A estrutura molecular do vermelho de fenol é dada por:
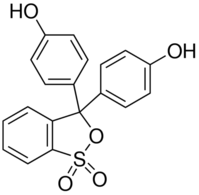
Estrutura molecular do vermelho de fenol
A mudança de coloração é decorrente do comportamento da molécula frente a mudança de pH. Isso ocorre devido ao fato de que o vermelho de fenol perde prótons com o aumento do pH. Em solução com pH muito baixo (ácido), o indicador é alaranjado e existe como um zwitterion, contendo tanto um grupo sulfato carregado negativamente quanto um grupo carbonila carregado positivamente. Caso o pH for aumentado, o próton do grupo carbonila carregado positivamente é perdido, resultando assim, em uma carregada negativamente. Aqui a coloração do indicador é amarela. Para valores de pH mais alcalinos os grupos hidroxílicos do fenol também perdem seus prótons, neste caso, o corante adquire a coloração fúcsia (Vermelho/rosa brilhante).
As reações que ocorrem são ilustradas na figura abaixo:
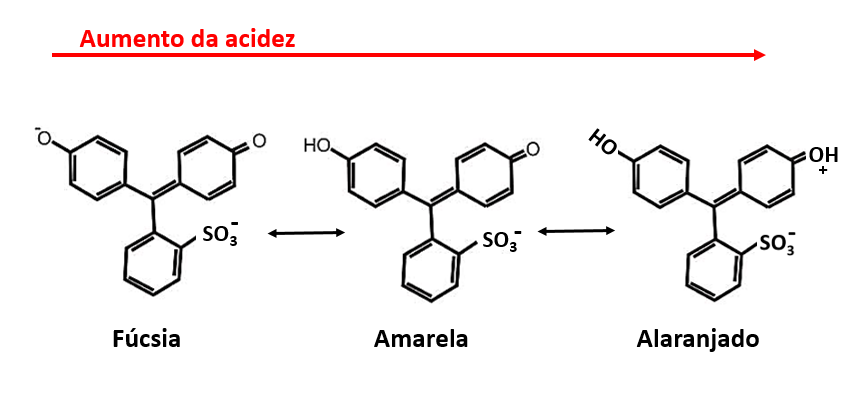
Etapas de desprotonação do corante
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
como ocorre o processo de protonacão e desprotonação de aminoácidos ?
Quimica e Bioquimica Estrutural
•FEF
Joao Vitor Flavio







Compartilhar