(UERJ 2014) A eletrólise da ureia, substância encontrada na urina, está sendo proposta como forma de obtenção de hidrogênio,
gás que pode ser utilizado como combustível. Observe as semirreações
da célula eletrolítica empregada nesse processo, realizado com 100% de rendimento:
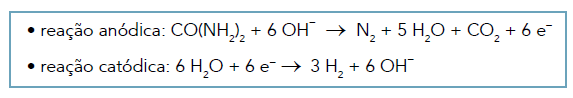
Considere as seguintes informações:
1 - A ureia tem fórmula química CO(NH\(_2\))\(_2\) e sua concentração na urina é de 20 g.L\(^{-1}\).
2 - Um ônibus movido a hidrogênio percorre 1 km com 100 g desse combustível.
Apresente a reação global da eletrólise da ureia. Em seguida, calcule a distância, em quilômetros, percorrida por um ônibus utilizando o combustível gerado na eletrólise de dez mil litros de urina.
💡 2 Respostas
Jose Augusto
CO(NH₂)₂ + H₂O → N² + CO² + 3H²
M = 1L .......................20 g
10.000 L.............. x g
x = 20 × 10⁵ g
CO(NH₂)₂ ........ 3H₂
60 g...................(3 ₓ 2g)
2 ₓ 10⁵ g.............. x
x = 2ₓ10⁴ g
100 gH₂ ........ 1km
2 ₓ 10⁴ gH₂ ...... s
s = 200 km
Estudante PD
Somando-se ambas as reações (catódica e anódica), obtêm-se a equação global:
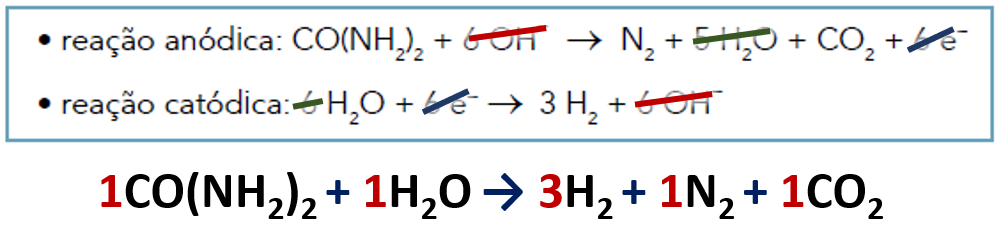
Para as grandezas envolvidas, utilizaremos "1" para hidrogênio e "2" para uréia!
Seja "c" o consumo de hidrogênio e "d" a distância:

Relação entre o número de mols de uréia e hidrogênio na reação global:
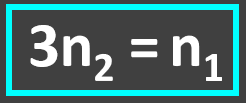
Relação entre mol, massa e massa molar:
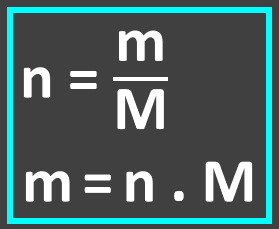
Relação entre as massas de hidrogênio e uréia:

Relação entre massa de uréia e volume de urina (através da concentração "C"):

Substituição na equação de "m1":
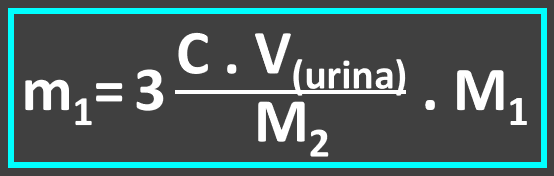
Substituindo "m1" na equação de "d", elaboramos a equação que solucinará o problema:
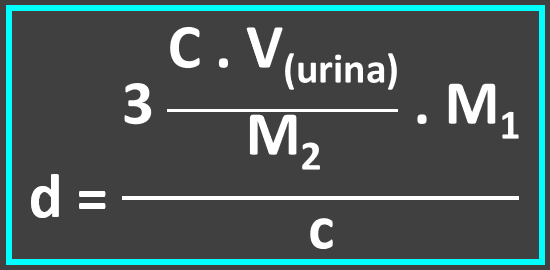
Inserção dos valores numéricos fornecidos (massas molares obtidas através da tabela periódica):


✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.





Compartilhar