Explique qual composto terá o ponto de ebulição mais alto, o cis-dicloro-eteno ou o trans-dicloro- eteno?
💡 1 Resposta
Matheus Bertolino Barros da Silva
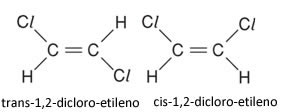
Precisamos analisar o momento dipolar de cada um. Devido à uma diferença de eletronegatividade, os átomos puxam/empurram uns aos outros. O cloro, em especial, possui uma eletronegatividade alta. Usando a figura de forma ilustrativa (onde temos o dicloro-etano), imagine que o cloro faz uma força puxando toda a estrutura de carbono e hidrogênio. No caso do isômero cis, essas forças se somam. No trans, elas se cancelam. Assim, pode-se concluir que o isômero cis tem momento dipolar mais forte. Se o momento dipolar é mais forte, as forças intermoleculares serão mais fortes. Se as forças intermoleculares são mais fortes, o ponto de ebulição é mais alto (pois a resistência das moléculas de se separar é maior). Portanto, o cis-dicloro-eteno terá PE mais alto.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 9 pág.
9 pág.



Compartilhar