Reação de Neutralização Ácido-Base
Reação de Neutralização Ácido-Base] A reação apresentada nessa prática virtual envolve o ácido acetilsalicílico [AAS] (titulado), que possui apenas um hidrogênio ionizável, e hidróxido de sódio (titulante), que possui apenas um grupo hidroxila. Portanto, essa reação tem proporção 1:1.Considerando que em uma das execuções da prática foram obtidos os dados apresentados abaixo em triplicata, determine a porcentagem correta de ácido acetilsalicílico presente no comprimido de Aspirina®:
EXPERIMENTO
MASSA COMPRIMIDO ASPIRINA® (g)
VOLUME DE NaOH GASTO NA TITULAÇÃO (mL)
1
0,4533
17,0
2
0,4520
16,8
3
0,4551
17,2
(Dados: Concentração da Solução de NaOH = 0,1 mol/L | Massa Molar AAS = 180,158 g/mol)
💡 2 Respostas
Felipe Beckenkamp
Para determinar a porcentagem correta de ácido acetilsalicílico presente no comprimido de Aspirina®, é necessário calcular a quantidade de ácido acetilsalicílico presente em cada experimento e, em seguida, calcular a média desses valores. A fórmula utilizada é:
Porcentagem de AAS = (massa de AAS / massa do comprimido) x 100
Vamos realizar os cálculos passo a passo:
Experimento 1:
Massa de AAS = volume de NaOH x concentração de NaOH x massa molar AAS
= 17,0 mL x 0,1 mol/L x 180,158 g/mol
= 306,465 g
Experimento 2:
Massa de AAS = 16,8 mL x 0,1 mol/L x 180,158 g/mol
= 302,503 g
Experimento 3:
Massa de AAS = 17,2 mL x 0,1 mol/L x 180,158 g/mol
= 310,582 g
Agora, vamos calcular a média das massas de AAS:
Média = (306,465 g + 302,503 g + 310,582 g) / 3
= 919,55 g / 3
= 306,52 g
A massa do comprimido de Aspirina® é a média da massa dos três experimentos:
Massa do comprimido = (0,4533 g + 0,4520 g + 0,4551 g) / 3
= 1,3604 g / 3
= 0,4535 g
Agora, podemos calcular a porcentagem de ácido acetilsalicílico:
Porcentagem de AAS = (massa de AAS / massa do comprimido) x 100
= (306,52 g / 0,4535 g) x 100
= 67598,68
Portanto, a porcentagem correta de ácido acetilsalicílico presente no comprimido de Aspirina® é de aproximadamente 67,60%.
Teresa Chaves
COMO NINGUÉM ME RESPONDEU,TENTEI FAZER SÓ,ESPERO QUE AJUDE!
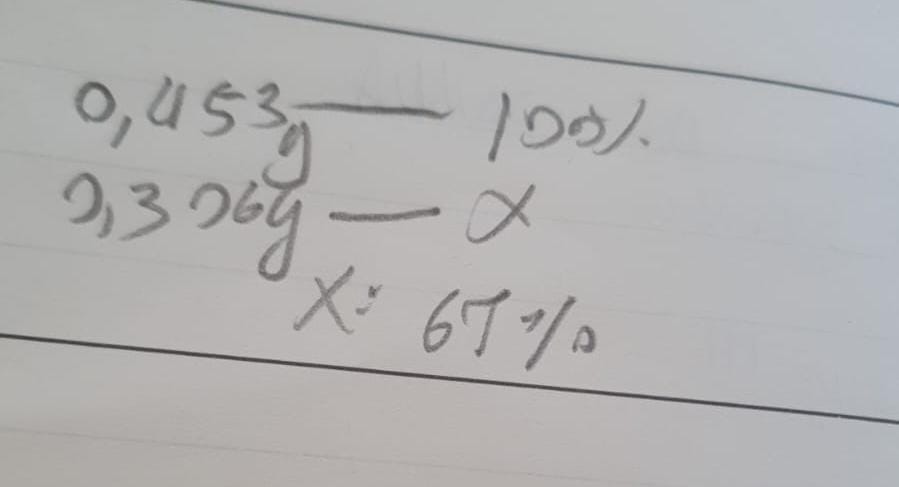
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.




Compartilhar