Respostas
sixbit t
http://www.vestibulardauerj.com.br/wp-content/uploads/2013/06/ex_disc_quimica.pdf
a resposta tá nesse link! Na questao 10.
Estudante PD
Reação química do processo:
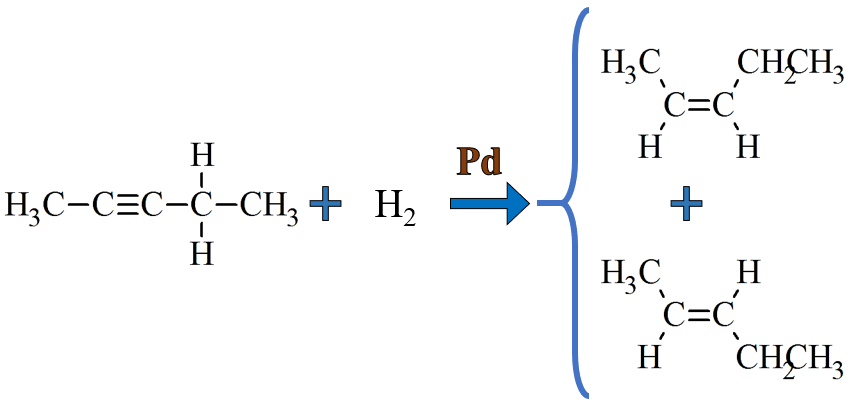
Abaixo, usaremos "1" para o pent-2-ino, "2" para o paládio e "3" para o hidrogênio!
Relação entre os volumes mencionados:
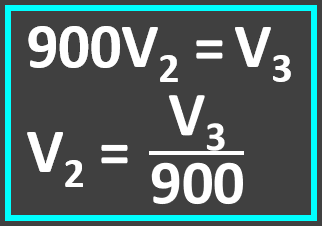
Relação entre densidade e massa do paládio:
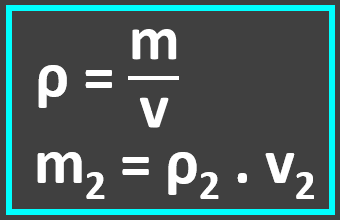
Relação entre densidade e volume de hidrogênio:

Relação entre paládio e hidrogênio:
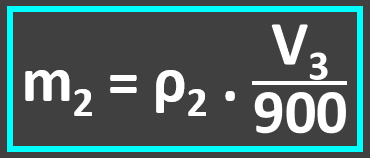
Equação I:
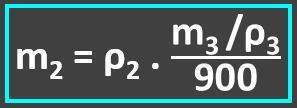
Relação entre hidrogênio e pent-2-ino (através da reação química demonstrada acima):
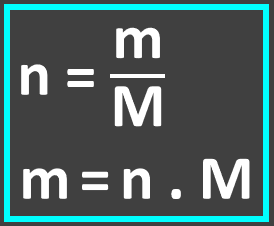
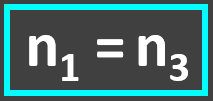
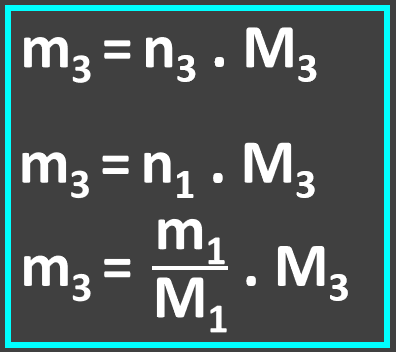
Substituindo na equação I, elaboramos a equação que solucionará o problema:
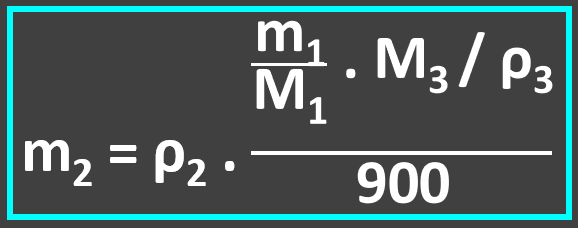
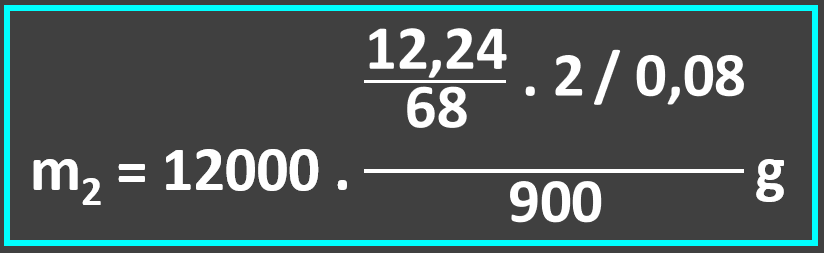
Ajustando a densidade do paládio para 12000 g/mL e, consultando a tabela periódica para as massas molares:

Fórmulas de bastão dos isômeros produzidos:
Cis-Pent-2-eno
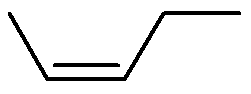
Trans-Pent-2-eno
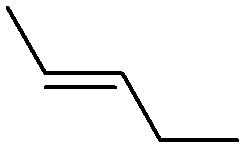
Responda
Para escrever sua resposta aqui, entre ou crie uma conta






